కీటోన్ బాడీస్ యొక్క బహుళ-డైమెన్షనల్ పాత్రలు
కీటోన్ శరీరాలు కాలేయం ద్వారా సృష్టించబడతాయి మరియు మానవ శరీరంలో గ్లూకోజ్ తక్షణమే అందుబాటులో లేనప్పుడు శక్తి వనరుగా ఉపయోగించబడుతుంది. రెండు ప్రధాన కీటోన్ శరీరాలు అసిటోఅసిటేట్ (AcAc) మరియు 3-బీటా-హైడ్రాక్సీబ్యూటిరేట్ (3HB), అయితే అసిటోన్ మూడవది మరియు అతి తక్కువ సమృద్ధిగా ఉండే కీటోన్ బాడీ. కీటోన్లు ఎల్లప్పుడూ రక్తంలో ఉంటాయి మరియు ఉపవాసం మరియు సుదీర్ఘ వ్యాయామం చేసేటప్పుడు వాటి స్థాయిలు పెరుగుతాయికీటోజెనిసిస్ కొవ్వు ఆమ్లాలు మరియు కీటోజెనిక్ అమైనో ఆమ్లాల విచ్ఛిన్నం ద్వారా జీవులు కీటోన్ శరీరాలను ఉత్పత్తి చేసే జీవరసాయన ప్రక్రియ.
కీటోన్ శరీరాలు ప్రధానంగా ఉత్పత్తి అవుతాయి కాలేయ కణాల మైటోకాండ్రియా. రక్తంలో తక్కువ గ్లూకోజ్ స్థాయిలు ఉన్నప్పుడు, ముఖ్యంగా గ్లైకోజెన్ వంటి ఇతర సెల్యులార్ కార్బోహైడ్రేట్ దుకాణాలు అయిపోయిన తర్వాత కీటోజెనిసిస్ సంభవిస్తుంది. ఇన్సులిన్ తగినంత మొత్తంలో లేనప్పుడు కూడా ఈ విధానం సంభవించవచ్చు. మానవ శరీరంలో కొవ్వు ఆమ్లాలుగా నిల్వ చేయబడిన శక్తిని అందుబాటులో ఉంచడానికి కీటోన్ శరీరాల ఉత్పత్తి చివరికి ప్రారంభించబడింది. కీటోజెనిసిస్ స్వతంత్రంగా నియంత్రించబడే మైటోకాండ్రియాలో సంభవిస్తుంది.
వియుక్త
కీటోన్ బాడీ మెటబాలిజం అనేది ఫిజియోలాజికల్ హోమియోస్టాసిస్లో కేంద్ర నోడ్. ఈ సమీక్షలో, వివిధ రకాల పోషక అవశేషాలలో అవయవం మరియు జీవి పనితీరును ఆప్టిమైజ్ చేసే మరియు బహుళ అవయవ వ్యవస్థలలో మంట మరియు గాయం నుండి రక్షించే వివిక్త చక్కటి-ట్యూనింగ్ జీవక్రియ పాత్రలను కీటోన్లు ఎలా అందిస్తాయో మేము చర్చిస్తాము. సాంప్రదాయకంగా కార్బోహైడ్రేట్ పరిమితిలో మాత్రమే నమోదు చేయబడిన జీవక్రియ సబ్స్ట్రేట్లుగా పరిగణించబడుతుంది, ఇటీవలి పరిశీలనలు కార్బోహైడ్రేట్లు సమృద్ధిగా ఉన్నప్పుడు కీటోన్ బాడీలు కీలకమైన జీవక్రియ మరియు సిగ్నలింగ్ మధ్యవర్తులుగా ప్రాముఖ్యతను నొక్కి చెబుతున్నాయి. నాడీ వ్యవస్థ యొక్క వ్యాధులకు తెలిసిన చికిత్సా ఎంపికల కచేరీలను పూర్తి చేయడం, క్యాన్సర్లో కీటోన్ శరీరాల కోసం భావి పాత్రలు పుట్టుకొచ్చాయి, గుండె మరియు కాలేయంలో చమత్కారమైన రక్షణ పాత్రలు ఉన్నాయి, ఊబకాయం-సంబంధిత మరియు హృదయ సంబంధ వ్యాధులలో చికిత్సా ఎంపికలను తెరవడం. కీటోన్ జీవక్రియ మరియు సిగ్నలింగ్లోని వివాదాలు సమకాలీన పరిశీలనలతో సాంప్రదాయ సిద్ధాంతాన్ని పునరుద్దరించటానికి చర్చించబడ్డాయి.
పరిచయం
కీటోన్ బాడీలు జీవితం, యూకారియా, బ్యాక్టీరియా మరియు ఆర్కియా యొక్క అన్ని డొమైన్లకు కీలకమైన ప్రత్యామ్నాయ జీవక్రియ ఇంధన వనరులు (అనెజా మరియు ఇతరులు, 2002; కాహిల్ GF Jr, 2006; కృష్ణకుమార్ మరియు ఇతరులు., 2008). మానవులలో కీటోన్ శరీర జీవక్రియ పోషకాహార లేమి యొక్క ఎపిసోడిక్ కాలాల్లో మెదడుకు ఇంధనంగా ఉపయోగపడుతుంది. కీటోన్ శరీరాలు కీలకమైన క్షీరద జీవక్రియ మార్గాలైన ?-ఆక్సిడేషన్ (FAO), ట్రైకార్బాక్సిలిక్ యాసిడ్ సైకిల్ (TCA), గ్లూకోనోజెనిసిస్, డి నోవో లిపోజెనిసిస్ (DNL) మరియు స్టెరాల్స్ బయోసింథసిస్ వంటి వాటితో ముడిపడి ఉంటాయి. క్షీరదాలలో, FAO-ఉత్పన్నమైన ఎసిటైల్-CoA నుండి కీటోన్ శరీరాలు ప్రధానంగా కాలేయంలో ఉత్పత్తి చేయబడతాయి మరియు అవి టెర్మినల్ ఆక్సీకరణ కోసం ఎక్స్ట్రాహెపాటిక్ కణజాలాలకు రవాణా చేయబడతాయి. ఈ శరీరధర్మ శాస్త్రం ప్రత్యామ్నాయ ఇంధనాన్ని అందిస్తుంది, ఇది సాపేక్షంగా క్లుప్త కాలాల ఉపవాసం ద్వారా వృద్ధి చెందుతుంది, ఇది కొవ్వు ఆమ్లాల లభ్యతను పెంచుతుంది మరియు కార్బోహైడ్రేట్ లభ్యతను తగ్గిస్తుంది (కాహిల్ GF Jr, 2006; McGarry and Foster, 1980; Robinson and Williamson, 1980). కీటోన్ బాడీ ఆక్సీకరణ ఉపవాసం, ఆకలి, నియోనాటల్ పీరియడ్, పోస్ట్-వ్యాయామం, గర్భం మరియు తక్కువ కార్బోహైడ్రేట్ ఆహారాలకు కట్టుబడి ఉండటం వంటి అనేక శారీరక స్థితులలో ఎక్స్ట్రాహెపాటిక్ కణజాలాలలో మొత్తం శక్తి క్షీరదాల జీవక్రియకు ముఖ్యమైన సహకారిగా మారుతుంది. ఆరోగ్యవంతమైన వయోజన మానవులలో మొత్తం కీటోన్ శరీర సాంద్రతలను ప్రసరించడం సాధారణంగా సుమారు 100–250 μM మధ్య సిర్కాడియన్ డోలనాలను ప్రదర్శిస్తుంది, సుదీర్ఘ వ్యాయామం లేదా 1 గంటల ఉపవాసం తర్వాత ~24 mM వరకు పెరుగుతుంది మరియు కీటోయాక్ డయాబెటిక్ వంటి వ్యాధికారక స్థితులలో 20 mM వరకు పేరుకుపోతుంది. కాహిల్ GF జూనియర్, 2006; జాన్సన్ మరియు ఇతరులు., 1969b; కోస్లాగ్ మరియు ఇతరులు., 1980; రాబిన్సన్ మరియు విలియమ్సన్, 1980; వైల్డెన్హాఫ్ మరియు ఇతరులు., 1974). మానవ కాలేయం రోజుకు 300 గ్రా కీటోన్ బాడీలను ఉత్పత్తి చేస్తుంది (బలాస్సే మరియు ఫెరీ, 1989), ఇది ఆహారం, ఉపవాసం మరియు ఆకలితో ఉన్న రాష్ట్రాలలో మొత్తం శక్తి వ్యయంలో 5-20% మధ్య దోహదపడుతుంది (బలాస్సే మరియు ఇతరులు, 1978; కాక్స్ మరియు అల్., 2016).
ఇటీవలి అధ్యయనాలు ఇప్పుడు క్షీరద కణ జీవక్రియ, హోమియోస్టాసిస్ మరియు అనేక రకాల శారీరక మరియు రోగలక్షణ స్థితులలో సిగ్నలింగ్లో కీటోన్ శరీరాల కోసం అత్యవసర పాత్రలను హైలైట్ చేస్తున్నాయి. మెదడు, గుండె లేదా అస్థిపంజర కండరం వంటి ఎక్స్ట్రాహెపాటిక్ కణజాలాలకు శక్తి ఇంధనాలుగా పనిచేయడమే కాకుండా, కీటోన్ బాడీలు సిగ్నలింగ్ మధ్యవర్తులుగా, ప్రొటీన్ పోస్ట్-ట్రాన్స్లేషనల్ మాడిఫికేషన్ (PTM) డ్రైవర్లుగా మరియు వాపు మరియు ఆక్సీకరణ ఒత్తిడికి మాడ్యులేటర్లుగా కీలక పాత్ర పోషిస్తాయి. ఈ సమీక్షలో, కీటోన్ బాడీస్ యొక్క ప్లియోట్రోపిక్ పాత్రలు మరియు వాటి జీవక్రియ యొక్క శాస్త్రీయ మరియు ఆధునిక వీక్షణలను మేము అందిస్తాము.
కీటోన్ బాడీ మెటబాలిజం యొక్క అవలోకనం
హెపాటిక్ కీటోజెనిసిస్ రేటు క్రొవ్వు యొక్క శారీరక మరియు జీవరసాయన పరివర్తనల యొక్క ఆర్కెస్ట్రేటెడ్ సిరీస్ ద్వారా నిర్వహించబడుతుంది. ప్రాథమిక నియంత్రకాలు ట్రయాసిల్గ్లిసరాల్స్ నుండి కొవ్వు ఆమ్లాల లిపోలిసిస్, హెపాటోసైట్ ప్లాస్మా పొరకు రవాణా చేయడం, కార్నిటైన్ పాల్మిటోయిల్ట్రాన్స్ఫేరేస్ 1 (CPT1) ద్వారా మైటోకాండ్రియాలోకి రవాణా చేయడం, ది ?-ఆక్సీకరణ స్పైరల్, TCA సైకిల్ యాక్టివిటీ మరియు ఇంటర్మీడియట్ రెడొరాక్స్ సంభావ్య సాంద్రతలు, రెగ్యులేటర్లు. ఈ ప్రక్రియలలో, ప్రధానంగా గ్లూకాగాన్ మరియు ఇన్సులిన్ [సమీక్షించబడింది (Arias et al., 1995; Ayte et al., 1993; Ehara et al., 2015; Ferre et al., 1983; Kahn et al., McGarry; 2005; Foster , 1980; విలియమ్సన్ మరియు ఇతరులు., 1969)]. సాంప్రదాయకంగా కీటోజెనిసిస్ ఒక స్పిల్ఓవర్ మార్గంగా పరిగణించబడుతుంది, దీనిలో ?-ఆక్సీకరణ-ఉత్పన్నమైన ఎసిటైల్-CoA సిట్రేట్ సింథేస్ కార్యాచరణ మరియు/లేదా సిట్రేట్ను ఏర్పరచడానికి సంగ్రహణ కోసం ఆక్సాలోఅసెటేట్ లభ్యతను మించిపోయింది. మూడు-కార్బన్ మధ్యవర్తులు యాంటీ-కెటోజెనిక్ చర్యను ప్రదర్శిస్తాయి, బహుశా అసిటైల్-CoA వినియోగం కోసం ఆక్సలోఅసెటేట్ పూల్ను విస్తరించే సామర్థ్యం కారణంగా, కానీ హెపాటిక్ అసిటైల్-CoA గాఢత మాత్రమే కీటోజెనిక్ రేటును నిర్ణయించదు (ఫోస్టర్, 1967; రావత్ మరియు మెనాహన్, 1975; మరియు ఇతరులు, 1969). హార్మోన్ల, ట్రాన్స్క్రిప్షనల్ మరియు పోస్ట్-ట్రాన్స్లేషనల్ ఈవెంట్ల ద్వారా కీటోజెనిసిస్ యొక్క నియంత్రణ కలిసి కీటోజెనిక్ రేటును చక్కగా మార్చే పరమాణు విధానాలు అసంపూర్తిగా అర్థం చేసుకోవడం అనే భావనకు మద్దతు ఇస్తుంది (HMGCS2 మరియు SCOT/OXCT1 నియంత్రణను చూడండి).
కీటోజెనిసిస్ ప్రాథమికంగా హెపాటిక్ మైటోకాన్డ్రియల్ మ్యాట్రిక్స్లో మొత్తం కొవ్వు ఆక్సీకరణకు అనులోమానుపాతంలో జరుగుతుంది. మైటోకాన్డ్రియాల్ పొరల మీదుగా ఎసిల్ చైన్ల రవాణా మరియు ?-ఆక్సిడేషన్ తర్వాత, 3-హైడ్రాక్సీమీథైల్గ్లుటరిల్-CoA సింథేస్ (HMGCS2) యొక్క మైటోకాన్డ్రియల్ ఐసోఫార్మ్ అసిటోఅసిటైల్-CoA (AcAc-CoGA- ఉత్పత్తి HAcAc-CotA) యొక్క సంక్షేపణకు కారణమయ్యే విధిని ఉత్ప్రేరకపరుస్తుంది. (Fig. 1A). HMG-CoA లైస్ (HMGCL) అసిటైల్-CoA మరియు అసిటోఅసిటేట్ (AcAc)ని విడుదల చేయడానికి HMG-CoAని క్లీవ్ చేస్తుంది మరియు రెండోది ఫాస్ఫాటిడైల్కోలిన్-ఆధారిత మైటోకాన్డ్రియల్ డిహైడ్రోజెన్ (HBB డీహైడ్రోజన్) ద్వారా d-?-hydroxybutyrate (d-?OHB)కి తగ్గించబడుతుంది. BDH1) ఒక NAD+/NADH-కపుల్డ్ నియర్-ఈక్విలిబ్రియం రియాక్షన్లో (బాక్ మరియు ఫ్లీషర్, 1975; LEHNINGER et al., 1960). BDH1 సమతౌల్య స్థిరాంకం d-?OHB ఉత్పత్తికి అనుకూలంగా ఉంటుంది, అయితే AcAc/d-?OHB కీటోన్ బాడీల నిష్పత్తి నేరుగా మైటోకాన్డ్రియల్ NAD+/NADH నిష్పత్తికి అనులోమానుపాతంలో ఉంటుంది, అందువలన BDH1 ఆక్సిడోరేడక్టేజ్ కార్యాచరణ మైటోకాన్డ్రియల్ రెడాక్స్ సంభావ్యతను మాడ్యులేట్ చేస్తుంది (Krebs, 1969.; విలియమ్సన్ మరియు ఇతరులు., 1967). AcAc ఆకస్మికంగా అసిటోన్కు డీకార్బాక్సిలేట్ అవుతుంది (పెడెర్సెన్, 1929), కీటోయాసిడోసిస్తో బాధపడుతున్న మానవులలో తీపి వాసనకు మూలం (అంటే, మొత్తం సీరం కీటోన్ బాడీలు > ~7 mM; AcAc pKa 3.6, ?OHB pKa 4.7). కీటోన్ శరీరాలను మైటోకాన్డ్రియల్ లోపలి పొర ద్వారా రవాణా చేసే విధానాలు తెలియవు, అయితే AcAc/d-?OHB కణాల నుండి మోనోకార్బాక్సిలేట్ ట్రాన్స్పోర్టర్ల ద్వారా విడుదల చేయబడుతుంది (క్షీరదాలలో, MCT 1 మరియు 2, దీనిని ద్రావణి క్యారియర్ 16A కుటుంబ సభ్యులు 1 అని కూడా పిలుస్తారు మరియు 7) మరియు టెర్మినల్ ఆక్సీకరణ కోసం ఎక్స్ట్రాహెపాటిక్ కణజాలాలకు ప్రసరణలో రవాణా చేయబడుతుంది (కోటర్ మరియు ఇతరులు, 2011; హాలెస్ట్రాప్ మరియు విల్సన్, 2012; హాలెస్ట్రాప్, 2012; హ్యూగో మరియు ఇతరులు., 2012). ప్రసరించే కీటోన్ శరీరాల సాంద్రతలు ఎక్స్ట్రాహెపాటిక్ కణజాలాలలో (హారిసన్ మరియు లాంగ్, 1940) కంటే ఎక్కువగా ఉంటాయి, ఇది కీటోన్ శరీరాలు ఏకాగ్రత ప్రవణతతో రవాణా చేయబడతాయని సూచిస్తున్నాయి. MCT1లోని లాస్-ఆఫ్-ఫంక్షన్ ఉత్పరివర్తనలు కీటోయాసిడోసిస్ యొక్క ఆకస్మిక పోరాటాలతో సంబంధం కలిగి ఉంటాయి, ఇది కీటోన్ బాడీ దిగుమతిలో కీలక పాత్రను సూచిస్తుంది.
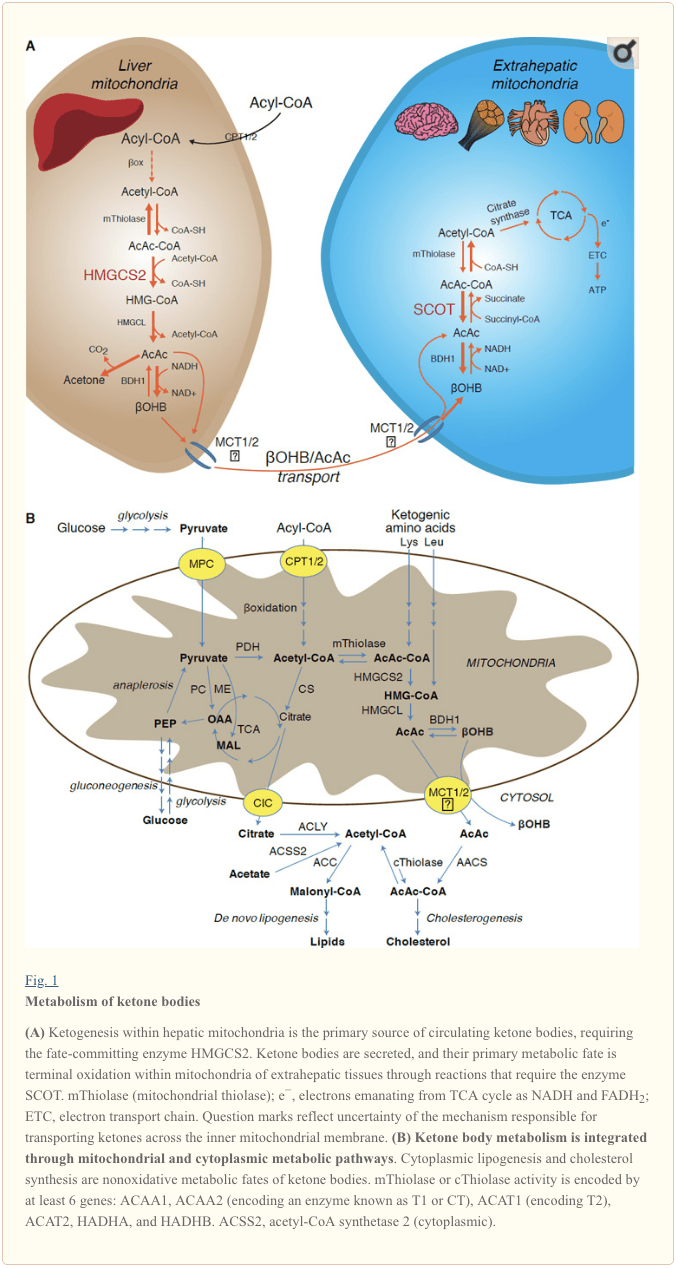
కీటోన్ శరీరాలను నాన్-ఆక్సిడేటివ్ ఫేట్స్లోకి మళ్లించడం మినహా (కీటోన్ బాడీస్ యొక్క నాన్-ఆక్సిడేటివ్ మెటబాలిక్ ఫేట్స్ చూడండి), హెపాటోసైట్లు అవి ఉత్పత్తి చేసే కీటోన్ బాడీలను జీవక్రియ చేసే సామర్థ్యాన్ని కలిగి ఉండవు. కాలేయం ద్వారా డి నోవో సంశ్లేషణ చేయబడిన కీటోన్ శరీరాలు (i) ఎక్స్ట్రాహెపాటిక్ కణజాలాల మైటోకాండ్రియాలో ఎసిటైల్-CoAకి ఉత్ప్రేరకమవుతాయి, ఇది TCA సైకిల్కి టెర్మినల్ ఆక్సీకరణ (Fig. 1A), (ii) లిపోజెనిసిస్ లేదా స్టెరాల్ సంశ్లేషణ మార్గాలకు మళ్లించబడుతుంది ( Fig. 1B), లేదా (iii) మూత్రంలో విసర్జించబడుతుంది. ప్రత్యామ్నాయ శక్తివంతమైన ఇంధనంగా, కీటోన్ శరీరాలు గుండె, అస్థిపంజర కండరం మరియు మెదడులో ఆక్సీకరణం చెందుతాయి (బలాస్సే మరియు ఫెరీ, 1989; బెంటోర్కియా మరియు ఇతరులు., 2009; ఓవెన్ మరియు ఇతరులు., 1967; రీచర్డ్ మరియు ఇతరులు., 1974; సుల్తాన్. ) ఎక్స్ట్రాహెపాటిక్ మైటోకాన్డ్రియల్ BDH1988 ?OHB ఆక్సీకరణ యొక్క మొదటి ప్రతిచర్యను ఉత్ప్రేరకపరుస్తుంది, దానిని బ్యాక్ AcAcగా మారుస్తుంది (LEHNINGER et al., 1; Sandermann et al., 1960). BDH1986కి కేవలం 2% సీక్వెన్స్ గుర్తింపు కలిగిన సైటోప్లాస్మిక్ d-?OHB-డీహైడ్రోజినేస్ (BDH20) కీటోన్ బాడీల కోసం అధిక కిమీని కలిగి ఉంటుంది మరియు ఐరన్ హోమియోస్టాసిస్లో కూడా పాత్ర పోషిస్తుంది (దావులూరి మరియు ఇతరులు, 1; గువో మరియు ఇతరులు., 2016) . ఎక్స్ట్రాహెపాటిక్ మైటోకాన్డ్రియల్ మ్యాట్రిక్స్లో, ప్రత్యేకమైన క్షీరదాల CoA ట్రాన్స్ఫేరేస్, succinyl-CoA:2006-oxoacid-CoA ట్రాన్స్ఫేరేస్ (SCOT, CoA ట్రాన్స్ఫేరేస్) ద్వారా ఉత్ప్రేరకమైన ప్రతిచర్యలో సక్సినైల్-CoA నుండి CoA-మోయిటీని మార్పిడి చేయడం ద్వారా AcAc AcAc-CoAకి సక్రియం చేయబడుతుంది; OXCT3 ద్వారా ఎన్కోడ్ చేయబడింది), సమీప సమతౌల్య ప్రతిచర్య ద్వారా. AcAc-CoA యొక్క జలవిశ్లేషణ ద్వారా విడుదలయ్యే ఉచిత శక్తి సక్సినైల్-CoA కంటే ఎక్కువగా ఉంటుంది, ఇది AcAc ఏర్పడటానికి అనుకూలంగా ఉంటుంది. అందువల్ల కీటోన్ బాడీ ఆక్సీకరణ ప్రవాహం మాస్ చర్య కారణంగా సంభవిస్తుంది: AcAc యొక్క సమృద్ధిగా సరఫరా మరియు సిట్రేట్ సింథేస్ ద్వారా ఎసిటైల్-CoA యొక్క వేగవంతమైన వినియోగం SCOT ద్వారా AcAc-CoA (+ సక్సినేట్) ఏర్పడటానికి అనుకూలంగా ఉంటుంది. ముఖ్యంగా, గ్లూకోజ్ (హెక్సోకినేస్) మరియు కొవ్వు ఆమ్లాలు (ఎసిల్-కోఏ సింథటేసెస్)కు విరుద్ధంగా, కీటోన్ బాడీలను (SCOT) ఆక్సిడైజ్ చేయదగిన రూపంలోకి క్రియాశీలం చేయడానికి ATP పెట్టుబడి అవసరం లేదు. రివర్సిబుల్ AcAc-CoA థియోలేస్ ప్రతిచర్య [ACAA1 (T2 లేదా CT అని పిలువబడే ఎంజైమ్ను ఎన్కోడింగ్ చేయడం), ACAT1 (ఎన్కోడింగ్ T1), HADHA లేదా HADHB ద్వారా ఎన్కోడ్ చేయబడిన నాలుగు మైటోకాన్డ్రియల్ థియోలేస్లలో దేనినైనా ఉత్ప్రేరకపరచడం వలన అసిటైల్-CoA యొక్క రెండు అణువులు లభిస్తాయి. ఇది TCA చక్రంలోకి ప్రవేశిస్తుంది (హెర్ష్ మరియు జెంక్స్, 2; స్టెర్న్ మరియు ఇతరులు, 1967; విలియమ్సన్ మరియు ఇతరులు., 1956). కీటోటిక్ స్థితులలో (అనగా, మొత్తం సీరం కీటోన్లు> 1971 μM), కీటోన్ శరీరాలు శక్తి వ్యయానికి గణనీయమైన సహాయకులుగా మారతాయి మరియు ఆక్సీకరణం తీసుకోవడం లేదా సంతృప్తత సంభవించే వరకు కణజాలాలలో వేగంగా ఉపయోగించబడతాయి (బాలాస్సే మరియు ఇతరులు, 500; బాలస్సే మరియు ఫెరీ, 1978 ; ఎడ్మండ్ మరియు ఇతరులు., 1989). కాలేయం-ఉత్పన్నమైన కీటోన్ శరీరాల యొక్క చాలా చిన్న భాగాన్ని మూత్రంలో సులభంగా కొలవవచ్చు మరియు మూత్రపిండాల ద్వారా వినియోగం మరియు పునశ్శోషణ రేట్లు ప్రసరణ ఏకాగ్రతకు అనులోమానుపాతంలో ఉంటాయి (గోల్డ్స్టెయిన్, 1987; రాబిన్సన్ మరియు విలియమ్సన్, 1987). అత్యంత కీటోటిక్ స్థితులలో (> 1980 mM ప్లాస్మాలో), కీటోనూరియా కీటోసిస్ యొక్క సెమీ-క్వాంటిటేటివ్ రిపోర్టర్గా పనిచేస్తుంది, అయినప్పటికీ మూత్ర కీటోన్ శరీరాల యొక్క చాలా క్లినికల్ పరీక్షలు AcAcని గుర్తించాయి కానీ ?OHB (క్లాకర్ మరియు ఇతరులు, 1).
కీటోజెనిక్ సబ్స్ట్రేట్లు మరియు హెపాటోసైట్ జీవక్రియపై వాటి ప్రభావం
కెటోజెనిక్ సబ్స్ట్రేట్లలో కొవ్వు ఆమ్లాలు మరియు అమైనో ఆమ్లాలు (Fig. 1B) ఉన్నాయి. అమైనో ఆమ్లాల ఉత్ప్రేరకము, ముఖ్యంగా లూసిన్, శోషించని స్థితిలో 4% కీటోన్ శరీరాలను ఉత్పత్తి చేస్తుంది (థామస్ మరియు ఇతరులు, 1982). అందువల్ల కీటోన్ శరీరాలను ఉత్పత్తి చేయడానికి ఎసిటైల్-CoA సబ్స్ట్రేట్ పూల్ ప్రధానంగా కొవ్వు ఆమ్లాల నుండి ఉద్భవించింది, ఎందుకంటే కార్బోహైడ్రేట్ సరఫరా తగ్గుతున్న సమయంలో, పైరువేట్ హెపాటిక్ TCA చక్రంలోకి ప్రధానంగా అనాప్లెరోసిస్ ద్వారా ప్రవేశిస్తుంది, అనగా ATP-ఆధారిత కార్బాక్సిలేషన్ నుండి ఆక్సాలోఅసెటేట్ (OAA), లేదా మాలేట్ వరకు. (MAL), మరియు అసిటైల్-CoAకి ఆక్సీకరణ డీకార్బాక్సిలేషన్ కాదు (జియోంగ్ మరియు ఇతరులు, 2012; మాగ్నస్సన్ మరియు ఇతరులు., 1991; మెరిట్ మరియు ఇతరులు., 2011). ఎసిటైల్-CoAకి పైరువేట్ డీకార్బాక్సిలేషన్ గరిష్టంగా ఉన్నప్పటికీ, కాలేయంలో, గ్లూకోజ్ మరియు పైరువేట్ కీటోజెనిసిస్కు చాలా తక్కువగా దోహదపడతాయి (జియోంగ్ మరియు ఇతరులు., 2012).
ఎసిటైల్-CoA టెర్మినల్ ఆక్సీకరణ ద్వారా ATP ఉత్పత్తికి మించి హెపాటిక్ మధ్యవర్తిత్వ జీవక్రియకు అనేక పాత్రలను కలిగి ఉంటుంది (కీటోన్ బాడీ మెటబాలిజం యొక్క ఏకీకరణ, పోస్ట్-ట్రాన్స్లేషనల్ సవరణ మరియు సెల్ ఫిజియాలజీని కూడా చూడండి). ఎసిటైల్-CoA అలోస్టెరికల్గా (i) పైరువేట్ కార్బాక్సిలేస్ (PC)ని సక్రియం చేస్తుంది, తద్వారా TCA చక్రంలో మెటాబోలైట్ల యొక్క అనాప్రోటిక్ ప్రవేశాన్ని పెంపొందించే జీవక్రియ నియంత్రణ యంత్రాంగాన్ని సక్రియం చేస్తుంది (ఓవెన్ మరియు ఇతరులు, 2002; స్క్రూటన్ మరియు అట్టర్, 1967) మరియు (ii) కినేస్, ఇది పైరువేట్ డీహైడ్రోజినేస్ (PDH)ని ఫాస్ఫోరైలేట్ చేస్తుంది మరియు నిరోధిస్తుంది (కూపర్ మరియు ఇతరులు, 1975), తద్వారా అనాప్లెరోసిస్ ద్వారా TCA చక్రంలోకి పైరువేట్ ప్రవాహాన్ని మరింత మెరుగుపరుస్తుంది. ఇంకా, సైటోప్లాస్మిక్ ఎసిటైల్-CoA, మైటోకాన్డ్రియల్ ఎసిటైల్-CoAను రవాణా చేయగల మెటాబోలైట్లుగా మార్చే మెకానిజమ్ల ద్వారా పెంచబడిన సైటోప్లాస్మిక్ ఎసిటైల్-CoA, కొవ్వు ఆమ్ల ఆక్సీకరణను నిరోధిస్తుంది: ఎసిటైల్-CoA కార్బాక్సిలేస్ (ACC) అసిటైల్-కోఎకి సబ్టైల్-కోఏగా మార్చడాన్ని ఉత్ప్రేరకపరుస్తుంది. మరియు మైటోకాన్డ్రియల్ CPT1 యొక్క అలోస్టెరిక్ ఇన్హిబిటర్ [(కాన్ మరియు ఇతరులు, 2005; మెక్గారీ మరియు ఫోస్టర్, 1980)లో సమీక్షించబడింది]. ఈ విధంగా, మైటోకాన్డ్రియల్ ఎసిటైల్-CoA పూల్ రెండూ కీటోజెనిసిస్ యొక్క స్పిల్ఓవర్ మార్గం ద్వారా నియంత్రించబడతాయి మరియు నియంత్రించబడతాయి, ఇది హెపాటిక్ మధ్యవర్తిత్వ జీవక్రియ యొక్క ముఖ్య అంశాలను ఆర్కెస్ట్రేట్ చేస్తుంది.
కీటోన్ బాడీస్ యొక్క నాన్-ఆక్సిడేటివ్ మెటబాలిక్ ఫేట్స్
కాలేయం-ఉత్పన్నమైన కీటోన్ల యొక్క ప్రధాన విధి SCOT-ఆధారిత ఎక్స్ట్రాహెపాటిక్ ఆక్సీకరణ. అయినప్పటికీ, AcAc మైటోకాండ్రియా నుండి ఎగుమతి చేయబడుతుంది మరియు సైటోప్లాస్మిక్ అసిటోఅసిటైల్-CoA సింథటేస్ (AACS, Fig. 1B) ద్వారా ఉత్ప్రేరకపరచబడిన ATP-ఆధారిత ప్రతిచర్య ద్వారా AcAc-CoAకి మార్చడం ద్వారా అనాబాలిక్ మార్గాలలో ఉపయోగించబడుతుంది. ఈ మార్గం మెదడు అభివృద్ధి సమయంలో మరియు పాలిచ్చే క్షీర గ్రంధిలో చురుకుగా ఉంటుంది (మోరిస్, 2005; రాబిన్సన్ మరియు విలియమ్సన్, 1978; ఓహ్గామి మరియు ఇతరులు., 2003). AACS కొవ్వు కణజాలం మరియు ఉత్తేజిత ఆస్టియోక్లాస్ట్లలో కూడా ఎక్కువగా వ్యక్తీకరించబడింది (అగ్యిలో మరియు ఇతరులు, 2010; యమసాకి మరియు ఇతరులు., 2016). సైటోప్లాస్మిక్ AcAc-CoAని సైటోసోలిక్ HMGCS1 ద్వారా స్టెరాల్ బయోసింథసిస్ వైపు మళ్లించవచ్చు లేదా రెండు సైటోప్లాస్మిక్ థియోలేస్లలో దేనితోనైనా అసిటైల్-CoA (ACAA1 మరియు ACAT2)కి మార్చవచ్చు, ఇది మలోనిల్-CoAకి కార్బాక్సిలేట్ చేయబడుతుంది మరియు కొవ్వు ఆమ్లాల సంశ్లేషణకు దోహదం చేస్తుంది. ఇతరులు, 1984; ఎడ్మండ్, 1974; ఎండెమాన్ మరియు ఇతరులు., 1982; గీలెన్ మరియు ఇతరులు., 1983; వెబ్బర్ మరియు ఎడ్మండ్, 1977).
శారీరక ప్రాముఖ్యత ఇంకా స్థాపించబడనప్పటికీ, కీటోన్లు కాలేయంలో కూడా అనాబాలిక్ సబ్స్ట్రేట్లుగా పనిచేస్తాయి. కృత్రిమ ప్రయోగాత్మక సందర్భాలలో, AcAc కొత్తగా సంశ్లేషణ చేయబడిన లిపిడ్లో సగం వరకు మరియు కొత్త సంశ్లేషణ కొలెస్ట్రాల్లో 75% వరకు దోహదపడుతుంది (ఎండెమాన్ మరియు ఇతరులు, 1982; గీలెన్ మరియు ఇతరులు., 1983; ఫ్రీడ్ మరియు ఇతరులు., 1988). AcAc అసంపూర్ణ హెపాటిక్ కొవ్వు ఆక్సీకరణ నుండి ఉద్భవించింది కాబట్టి, వివోలో లిపోజెనిసిస్కు దోహదపడే AcAc సామర్థ్యం హెపాటిక్ వ్యర్థమైన సైక్లింగ్ను సూచిస్తుంది, ఇక్కడ కొవ్వు-ఉత్పన్నమైన కీటోన్లను లిపిడ్ ఉత్పత్తికి ఉపయోగించవచ్చు, దీని శారీరక ప్రాముఖ్యత ప్రయోగాత్మక ధ్రువీకరణ అవసరం, కానీ ఉపయోగపడుతుంది. అనుకూల లేదా దుర్వినియోగ పాత్రలు (సోలినాస్ మరియు ఇతరులు, 2015). AcAc తక్కువ AACS Km-AcAc (~50 ~M)తో కొలెస్టెరోజెనిసిస్ను సరఫరా చేస్తుంది, ఫెడ్ స్టేట్లో కూడా AcAc యాక్టివేషన్కు అనుకూలంగా ఉంటుంది (బెర్గ్స్ట్రోమ్ మరియు ఇతరులు., 1984). సైటోప్లాస్మిక్ కీటోన్ జీవక్రియ యొక్క డైనమిక్ పాత్ర ప్రైమరీ మౌస్ ఎంబ్రియోనిక్ న్యూరాన్లలో మరియు 3T3-L1 డెరైవ్డ్-అడిపోసైట్స్లో సూచించబడింది, AACS నాక్డౌన్ ప్రతి కణ రకం యొక్క భేదాన్ని బలహీనపరిచింది (హసెగావా మరియు ఇతరులు, 2012a; హసేగావా మరియు 2012 al.). వివోలో ఎలుకలలో AACS యొక్క నాక్డౌన్ సీరం కొలెస్ట్రాల్ను తగ్గించింది (హసెగావా మరియు ఇతరులు., 2012c). SREBP-2, కొలెస్ట్రాల్ బయోసింథసిస్ యొక్క మాస్టర్ ట్రాన్స్క్రిప్షనల్ రెగ్యులేటర్ మరియు పెరాక్సిసోమ్ ప్రొలిఫెరేటర్ యాక్టివేటెడ్ రిసెప్టర్ (PPAR)-? AACS ట్రాన్స్క్రిప్షనల్ యాక్టివేటర్లు, మరియు న్యూరైట్ డెవలప్మెంట్ సమయంలో మరియు కాలేయంలో దాని ట్రాన్స్క్రిప్షన్ను నియంత్రిస్తాయి (అగ్యిలో మరియు ఇతరులు, 2010; హసెగావా మరియు ఇతరులు., 2012c). కలిసి తీసుకుంటే, సైటోప్లాస్మిక్ కీటోన్ బాడీ మెటబాలిజం ఎంపిక చేయబడిన పరిస్థితులు లేదా వ్యాధి సహజ చరిత్రలలో ముఖ్యమైనది కావచ్చు, కానీ కాలేయం-ఉత్పన్నమైన కీటోన్ బాడీలను పారవేసేందుకు సరిపోదు, ఎందుకంటే పనితీరు ఉత్పరివర్తనలు కోల్పోవడం ద్వారా ప్రాధమిక ఆక్సీకరణ విధి యొక్క ఎంపిక బలహీనత నేపథ్యంలో భారీ హైపర్కెటోనిమియా ఏర్పడుతుంది. SCOT కు (బెర్రీ మరియు ఇతరులు, 2001; కాటర్ మరియు ఇతరులు., 2011).
HMGCS2 మరియు SCOT/OXCT1 యొక్క నియంత్రణ
జీన్ ఎన్కోడింగ్ సైటోసోలిక్ హెచ్ఎమ్జిసిఎస్ నుండి మైటోకాన్డ్రియల్ యొక్క వైరుధ్యం సకశేరుక పరిణామంలో ప్రారంభంలోనే సంభవించింది, ఇది అధిక మెదడు నుండి శరీర బరువు నిష్పత్తులతో కూడిన జాతులలో హెపాటిక్ కీటోజెనిసిస్కు మద్దతు ఇవ్వాల్సిన అవసరం ఏర్పడింది (బౌకాఫ్టేన్ మరియు ఇతరులు, 1994; కున్నాన్ మరియు క్రాఫోర్డ్, 2003). మానవులలో సహజంగా సంభవించే లాస్-ఆఫ్-ఫంక్షన్ HMGCS2 ఉత్పరివర్తనలు హైపోకెటోటిక్ హైపోగ్లైసీమియాకు కారణమవుతాయి (పిట్ మరియు ఇతరులు, 2015; థాంప్సన్ మరియు ఇతరులు., 1997). బలమైన HMGCS2 వ్యక్తీకరణ హెపాటోసైట్లు మరియు పెద్దప్రేగు ఎపిథీలియంకు పరిమితం చేయబడింది మరియు దాని వ్యక్తీకరణ మరియు ఎంజైమాటిక్ కార్యకలాపాలు విభిన్న యంత్రాంగాల ద్వారా సమన్వయం చేయబడతాయి (మస్కారో మరియు ఇతరులు, 1995; మెక్గారీ మరియు ఫోస్టర్, 1980; రాబిన్సన్ మరియు విలియమ్సన్, 1980). HMGCS2ని ప్రభావితం చేసే శారీరక స్థితి యొక్క పూర్తి పరిధికి మరింత స్పష్టత అవసరం అయితే, దాని వ్యక్తీకరణ మరియు/లేదా కార్యాచరణ ప్రారంభ ప్రసవానంతర కాలంలో, వృద్ధాప్యం, మధుమేహం, ఆకలి లేదా కీటోజెనిక్ ఆహారం తీసుకోవడం (బలాస్సే మరియు ఫెరీ, 1989; కాహిల్ GF Jr, 2006) సమయంలో నియంత్రించబడుతుంది. ; గిరార్డ్ మరియు ఇతరులు., 1992; హెగార్డ్, 1999; సతపతి మరియు ఇతరులు., 2012; సేన్గుప్తా మరియు ఇతరులు., 2010). పిండంలో, Hmgcs5 జన్యువు యొక్క 2− పార్శ్వ ప్రాంతం యొక్క మిథైలేషన్ దాని లిప్యంతరీకరణతో విలోమ సహసంబంధం కలిగి ఉంటుంది మరియు పుట్టిన తర్వాత పాక్షికంగా తిరగబడుతుంది (Arias et al., 1995; Ayte et al., 1993; Ehara et al., 2015; Ferreet ; ., 1983). అదేవిధంగా, హెపాటిక్ Bdh1 అభివృద్ధి వ్యక్తీకరణ నమూనాను ప్రదర్శిస్తుంది, పుట్టినప్పటి నుండి ఈనిన వరకు పెరుగుతుంది మరియు ఫైబ్రోబ్లాస్ట్ గ్రోత్ ఫ్యాక్టర్ (FGF)-21-ఆధారిత పద్ధతిలో కీటోజెనిక్ డైట్ ద్వారా కూడా ప్రేరేపించబడుతుంది (బాడ్మాన్ మరియు ఇతరులు, 2007; జాంగ్ మరియు ఇతరులు., 1989 ) క్షీరదాలలోని కీటోజెనిసిస్ ఇన్సులిన్ మరియు గ్లూకాగాన్ రెండింటికి అత్యంత ప్రతిస్పందిస్తుంది, వరుసగా అణచివేయబడుతుంది మరియు ప్రేరేపించబడుతుంది (మెక్గారీ మరియు ఫోస్టర్, 1977). ఇన్సులిన్ కొవ్వు కణజాల లిపోలిసిస్ను అణిచివేస్తుంది, తద్వారా దాని ఉపరితలం యొక్క కీటోజెనిసిస్ను కోల్పోతుంది, అయితే గ్లూకాగాన్ కాలేయంపై ప్రత్యక్ష ప్రభావం ద్వారా కీటోజెనిక్ ఫ్లక్స్ను పెంచుతుంది (హెగార్డ్ట్, 1999). Hmgcs2 ట్రాన్స్క్రిప్షన్ ఫోర్క్హెడ్ ట్రాన్స్క్రిప్షనల్ ఫ్యాక్టర్ FOXA2 ద్వారా ప్రేరేపించబడుతుంది, ఇది ఇన్సులిన్-ఫాస్ఫాటిడైలినోసిటాల్-3-కినేస్/Akt ద్వారా నిరోధించబడుతుంది మరియు గ్లూకాగాన్-cAMP-p300 సిగ్నలింగ్ ద్వారా ప్రేరేపించబడుతుంది (Arias et al., 1995t. . PPAR? (రోడ్రిగ్జ్ మరియు ఇతరులు, 1994) దాని లక్ష్యం, FGF21 (బ్యాడ్మాన్ మరియు ఇతరులు, 2007) కలిసి ఆకలితో ఉన్నప్పుడు లేదా కీటోజెనిక్ డైట్ (బాడ్మ్యాన్ మరియు ఇతరులు, 2; ఇనాగాకి 2007, ఇనాగాకి 2007 et al. ) PPAR యొక్క ప్రేరణ? పిండం నుండి నియోనాటల్ ఫిజియాలజీకి మారడానికి ముందు సంభవించవచ్చు, అయితే ?OHB-మధ్యవర్తిత్వ నిరోధం హిస్టోన్ డీసిటైలేస్ (HDAC)-21 (రాండో మరియు ఇతరులు, 3) ద్వారా ప్రారంభ నియోనాటల్ పీరియడ్లో FGF2016 యాక్టివేషన్ అనుకూలంగా ఉండవచ్చు. mTORC1 (రాపామైసిన్ కాంప్లెక్స్ 1 యొక్క క్షీరదాల లక్ష్యం) PPAR యొక్క ఆధారిత నిరోధం? ట్రాన్స్క్రిప్షనల్ యాక్టివిటీ అనేది Hmgcs2 జన్యు వ్యక్తీకరణ (సెన్గుప్తా మరియు ఇతరులు, 2010) యొక్క కీలక నియంత్రకం, మరియు కాలేయం PER2, ఒక మాస్టర్ సిర్కాడియన్ ఓసిలేటర్, Hmgcs2 వ్యక్తీకరణను పరోక్షంగా నియంత్రిస్తుంది (చవాన్ మరియు ఇతరులు, 2016). ఇటీవలి పరిశీలనలు ఎక్స్ట్రాహెపాటిక్ ట్యూమర్-ప్రేరిత ఇంటర్లుకిన్-6 PPAR ద్వారా కీటోజెనిసిస్ను బలహీనపరుస్తుందని సూచిస్తున్నాయి? అణచివేత (ఫ్లింట్ మరియు ఇతరులు, 2016).
HMGCS2 ఎంజైమ్ కార్యాచరణ బహుళ PTMల ద్వారా నియంత్రించబడుతుంది. HMGCS2 సెరైన్ ఫాస్ఫోరైలేషన్ దాని కార్యాచరణను విట్రోలో మెరుగుపరిచింది (గ్రిమ్స్రుడ్ మరియు ఇతరులు., 2012). HMGCS2 కార్యాచరణ సక్సినైల్-CoA మరియు లైసిన్ అవశేషాల సక్సినైలేషన్ ద్వారా అలోస్టెరికల్గా నిరోధించబడుతుంది (అరియాస్ మరియు ఇతరులు, 1995; హెగార్డ్, 1999; లోవ్ మరియు టబ్స్, 1985; క్వాంట్ మరియు ఇతరులు, 1990; రాడిన్, etal. 2013, etal. 1975; థుమెలిన్ మరియు ఇతరులు., 1993). హెపాటిక్ మైటోకాండ్రియాలోని HMGCS2, HMGCL మరియు BDH1 లైసిన్ అవశేషాల సక్సినైలేషన్ NAD+ ఆధారిత డీసైలేస్ సిర్టుయిన్ 5 (SIRT5) (రార్డిన్ మరియు ఇతరులు, 2013) యొక్క లక్ష్యాలు. HMGCS2 కార్యాచరణ కూడా SIRT3 లైసిన్ డీసీటైలేషన్ ద్వారా మెరుగుపరచబడింది మరియు ఎసిటైలేషన్ మరియు సక్సినైలేషన్ మధ్య క్రాస్స్టాక్ HMGCS2 కార్యాచరణను నియంత్రిస్తుంది (రార్డిన్ మరియు ఇతరులు, 2013; షిమాజు మరియు ఇతరులు., 2013). HMGCS2 Km మరియు Vmaxని నియంత్రించడానికి ఈ PTMల సామర్థ్యం ఉన్నప్పటికీ, ఈ PTMల హెచ్చుతగ్గులు ఇంకా జాగ్రత్తగా మ్యాప్ చేయబడలేదు మరియు vivoలో కీటోజెనిసిస్ యొక్క మెకానిస్టిక్ డ్రైవర్లుగా నిర్ధారించబడలేదు.
హెపటోసైట్లు మినహా మైటోకాండ్రియాను కలిగి ఉన్న అన్ని క్షీరద కణాలలో SCOT వ్యక్తీకరించబడుతుంది. SCOT కార్యాచరణ మరియు కీటోలిసిస్ యొక్క ప్రాముఖ్యత SCOT-KO ఎలుకలలో ప్రదర్శించబడింది, ఇది పుట్టిన తర్వాత 48 గంటలలోపు హైపర్కెటోనెమిక్ హైపోగ్లైసీమియా కారణంగా ఏకరీతి ప్రాణాంతకతను ప్రదర్శించింది (కోటర్ మరియు ఇతరులు., 2011). న్యూరాన్లు లేదా అస్థిపంజర మయోసైట్లలో SCOT యొక్క కణజాల-నిర్దిష్ట నష్టం ఆకలితో ఉన్నప్పుడు జీవక్రియ అసాధారణతలను ప్రేరేపిస్తుంది కానీ ప్రాణాంతకం కాదు (కోటర్ మరియు ఇతరులు, 2013b). మానవులలో, SCOT లోపం తీవ్రమైన కీటోయాసిడోసిస్తో ప్రారంభ దశలో ఉంటుంది, ఇది బద్ధకం, వాంతులు మరియు కోమాకు కారణమవుతుంది (బెర్రీ et al., 2001; Fukao et al., 2000; Kassovska-Bratinova et al., 1996; Niezen-Kaloning. , 1997; సౌదుబ్రే మరియు ఇతరులు., 1987; స్నైడెర్మాన్ మరియు ఇతరులు., 1998; టిల్డన్ మరియు కార్న్బ్లాత్, 1972). SCOT జన్యువు మరియు ప్రోటీన్ వ్యక్తీకరణ నియంత్రకాల గురించి సెల్యులార్ స్థాయిలో చాలా తక్కువగా తెలుసు. Oxct1 mRNA వ్యక్తీకరణ మరియు SCOT ప్రోటీన్ మరియు కార్యకలాపాలు కీటోటిక్ స్థితులలో తగ్గిపోతాయి, బహుశా PPAR-ఆధారిత మెకానిజమ్ల ద్వారా (ఫెన్సేలౌ మరియు వాలిస్, 1974; ఫెన్సేలౌ మరియు వాలిస్, 1976; గ్రిన్బ్లాట్ మరియు ఇతరులు., 1986; ఓకుడా మరియు ఇతరులు., 1991etal. ., 2001; వెంట్జ్ మరియు ఇతరులు., 2010). డయాబెటిక్ కీటోయాసిడోసిస్లో, హెపాటిక్ కీటోజెనిసిస్ మరియు ఎక్స్ట్రాహెపాటిక్ ఆక్సీకరణ మధ్య అసమతుల్యత SCOT కార్యకలాపాల బలహీనత ద్వారా తీవ్రమవుతుంది. కార్డియోమయోసైట్స్లో ఇన్సులిన్-ఇండిపెండెంట్ గ్లూకోజ్ ట్రాన్స్పోర్టర్ (GLUT1/SLC2A1) యొక్క అతిగా ఎక్స్ప్రెషన్ కూడా Oxct1 జన్యు వ్యక్తీకరణను నిరోధిస్తుంది మరియు నాన్-కెటోటిక్ స్థితిలో కీటోన్స్ టెర్మినల్ ఆక్సీకరణను తగ్గిస్తుంది (యాన్ మరియు ఇతరులు, 2009). కాలేయంలో, Oxct1 mRNA సమృద్ధి మైక్రోఆర్ఎన్ఎ-122 మరియు హిస్టోన్ మిథైలేషన్ H3K27me3 ద్వారా అణచివేయబడుతుంది, ఇవి పిండం నుండి నియోనాటల్ పీరియడ్కి మారే సమయంలో స్పష్టంగా కనిపిస్తాయి (థోర్రేజ్ మరియు ఇతరులు., 2011). ఏది ఏమైనప్పటికీ, ప్రసవానంతర కాలంలో హెపాటిక్ Oxct1 వ్యక్తీకరణను అణచివేయడం అనేది ప్రాథమికంగా కాలేయం నుండి Oxct1-వ్యక్తీకరించే హెమటోపోయిటిక్ ప్రొజెనిటర్లను తరలించడం, అంతకుముందు ఉన్న Oxct1 వ్యక్తీకరణను టెర్మినల్ డిఫరెన్సియేటెడ్ హెపటోసైట్లలో కోల్పోవడం కంటే ప్రధానంగా చెప్పవచ్చు. వాస్తవానికి, విభిన్న హెపటోసైట్లలో Oxct1 mRNA మరియు SCOT ప్రోటీన్ యొక్క వ్యక్తీకరణ చాలా తక్కువగా ఉంటుంది (Orii et al., 2008).
SCOT కూడా PTMలచే నియంత్రించబడుతుంది. ఎంజైమ్ SIRT3 KO ఎలుకల మెదడుల్లో హైపర్-ఎసిటైలేట్ చేయబడింది, ఇది తగ్గిన AcAc ఆధారిత ఎసిటైల్-CoA ఉత్పత్తిని కూడా ప్రదర్శిస్తుంది (డిట్టెన్హాఫర్-రీడ్ మరియు ఇతరులు., 2015). SCOT యొక్క టైరోసిన్ అవశేషాల యొక్క నాన్-ఎంజైమాటిక్ నైట్రేషన్ దాని కార్యాచరణను కూడా పెంచుతుంది, ఇది వివిధ డయాబెటిక్ ఎలుకల నమూనాల హృదయాలలో నివేదించబడింది (మార్కోండెస్ మరియు ఇతరులు, 2001; టర్కో మరియు ఇతరులు., 2001; వాంగ్ మరియు ఇతరులు., 2010a). దీనికి విరుద్ధంగా, ట్రిప్టోఫాన్ అవశేష నైట్రేషన్ SCOT కార్యాచరణను పెంచుతుంది (Brg're et al., 2010; Rebrin et al., 2007). SCOT కార్యాచరణను మాడ్యులేట్ చేయడానికి రూపొందించబడిన అవశేష-నిర్దిష్ట నైట్రేషన్ లేదా డి-నైట్రేషన్ యొక్క పరమాణు విధానాలు ఉండవచ్చు మరియు స్పష్టీకరణ అవసరం.
ఎక్స్ట్రాహెపాటిక్ కీటోజెనిసిస్లో వివాదాలు
క్షీరదాలలో ప్రాథమిక కీటోజెనిక్ అవయవం కాలేయం, మరియు హెపటోసైట్లు మరియు గట్ ఎపిథీలియల్ కణాలు మాత్రమే HMGCS2 యొక్క మైటోకాన్డ్రియల్ ఐసోఫార్మ్ను సమృద్ధిగా వ్యక్తీకరిస్తాయి (కోటర్ మరియు ఇతరులు, 2013a; కాటర్ మరియు ఇతరులు., 2014; మెక్గారీ మరియు ఫోస్టర్, 1980; రోబిన్సన్, 1980; . కాంప్లెక్స్ పాలిసాకరైడ్ల వాయురహిత బాక్టీరియా కిణ్వ ప్రక్రియ బ్యూటిరేట్ను అందిస్తుంది, ఇది టెర్మినల్ ఆక్సీకరణ లేదా కీటోజెనిసిస్ (చెర్బుయ్ మరియు ఇతరులు, 1995) కోసం క్షీరదాలలోని కొలనోసైట్లచే శోషించబడుతుంది, ఇది కొలనోసైట్ భేదంలో పాత్ర పోషిస్తుంది (వాంగ్ మరియు ఇతరులు., 2016). గట్ ఎపిథీలియల్ కణాలు మరియు హెపటోసైట్లను మినహాయించి, దాదాపు అన్ని ఇతర క్షీరద కణాలలో HMGCS2 దాదాపుగా లేదు, అయితే కణితి కణాలు, కేంద్ర నాడీ వ్యవస్థ యొక్క ఆస్ట్రోసైట్లు, మూత్రపిండాలు, ప్యాంక్రియాటిక్లలో ఎక్స్ట్రాహెపాటిక్ కీటోజెనిసిస్ సంభావ్యత పెరిగింది? కణాలు, రెటీనా పిగ్మెంట్ ఎపిథీలియం (RPE), మరియు అస్థిపంజర కండరంలో కూడా (అడిజాంటో మరియు ఇతరులు, 2014; అవోగారో మరియు ఇతరులు., 1992; ఎల్ అజోనీ మరియు ఇతరులు., 2016; గ్రాబాకా మరియు ఇతరులు., 2016; కాంగ్ 2015, ; లే ఫోల్ మరియు ఇతరులు., 2014; నోనాకా మరియు ఇతరులు., 2016; తకాగి మరియు ఇతరులు., 2016a; థెవెనెట్ మరియు ఇతరులు., 2016; జాంగ్ మరియు ఇతరులు., 2011). నికర కీటోజెనిక్ సామర్థ్యం లేని కణజాలాలలో ఎక్టోపిక్ HMGCS2 గమనించబడింది (కుక్ మరియు ఇతరులు, 2016; వెంట్జ్ మరియు ఇతరులు., 2010), మరియు HMGCS2 సెల్ న్యూక్లియస్తో సహా భావి కీటోజెనిసిస్-స్వతంత్ర మూన్లైటింగ్ కార్యకలాపాలను ప్రదర్శిస్తుంది (చెన్ మొదలైనవి. , 2016; కోస్టియుక్ మరియు ఇతరులు., 2010; మీర్టెన్స్ మరియు ఇతరులు., 1998).
కీటోన్ బాడీలను ఆక్సీకరణం చేసే ఏదైనా ఎక్స్ట్రాహెపాటిక్ కణజాలం కూడా HMGCS2 ఇండిపెండెంట్ మెకానిజమ్స్ (Fig. 2A) ద్వారా కీటోన్ బాడీలను కూడబెట్టుకునే సామర్థ్యాన్ని కలిగి ఉంటుంది. ఏదేమైనప్పటికీ, రక్తప్రసరణలో ఉండే స్థిరమైన కీటోన్ బాడీ ఏకాగ్రత (కోటర్ మరియు ఇతరులు, 2011; కాటర్ మరియు ఇతరులు, 2013b; హారిసన్ మరియు లాంగ్, 1940) కంటే ఎక్కువగా ఉండే ఎక్స్ట్రాహెపాటిక్ కణజాలం లేదు. MCT1/2-ఆధారిత మెకానిజమ్స్ ద్వారా ఏకాగ్రత ప్రవణత. స్పష్టమైన ఎక్స్ట్రాహెపాటిక్ కీటోజెనిసిస్ యొక్క ఒక విధానం వాస్తవానికి కీటోన్ ఆక్సీకరణ యొక్క సాపేక్ష బలహీనతను ప్రతిబింబిస్తుంది. అదనపు సంభావ్య వివరణలు కీటోన్ బాడీ ఫార్మేషన్ పరిధిలోకి వస్తాయి. మొదట, డి నోవో కీటోజెనిసిస్ థియోలేస్ మరియు SCOT యొక్క రివర్సిబుల్ ఎంజైమాటిక్ చర్య ద్వారా సంభవించవచ్చు (వీడెమాన్ మరియు క్రెబ్స్, 1969). ఎసిటైల్-CoA యొక్క సాంద్రత సాపేక్షంగా ఎక్కువగా ఉన్నప్పుడు, సాధారణంగా AcAc ఆక్సీకరణకు కారణమయ్యే ప్రతిచర్యలు రివర్స్ దిశలో పనిచేస్తాయి (GOLDMAN, 1954). TCA సైకిల్ అడ్డంకి కారణంగా ?-ఆక్సీకరణ-ఉత్పన్నమైన మధ్యవర్తులు పేరుకుపోయినప్పుడు రెండవ మెకానిజం ఏర్పడుతుంది, మైటోకాన్డ్రియల్ 3-హైడ్రాక్సీసైసిల్-CoA డీహైడ్రోజినేస్ ద్వారా ఉత్ప్రేరకపరచబడిన ప్రతిచర్య ద్వారా AcAc-CoA l-?OHB-CoAగా మార్చబడుతుంది మరియు 3-హైడ్రాక్సీబ్యూటరిల్ ద్వారా CoA deacylase to l-?OHB, ఇది ఫిజియోలాజికల్ ఎన్యాంటియోమర్ d-?OHB (రీడ్ మరియు ఓజాండ్, 1980) నుండి మాస్ స్పెక్ట్రోమెట్రీ లేదా రెసొనెన్స్ స్పెక్ట్రోస్కోపీ ద్వారా వేరు చేయలేనిది. l-?OHBని క్రోమాటోగ్రాఫికల్గా లేదా ఎంజైమ్గా d-?OHB నుండి వేరు చేయవచ్చు మరియు ఇది ఎక్స్ట్రాహెపాటిక్ కణజాలాలలో ఉంటుంది, కానీ కాలేయం లేదా రక్తంలో కాదు (Hsu et al., 2011). హెపాటిక్ కీటోజెనిసిస్ d-?OHBని మాత్రమే ఉత్పత్తి చేస్తుంది, ఇది BDH సబ్స్ట్రేట్ అయిన ఏకైక ఎన్యాంటియోమర్ (ఇటో మరియు ఇతరులు, 1984; లింకన్ మరియు ఇతరులు., 1987; రీడ్ మరియు ఓజాండ్, 1980; స్కోఫీల్డ్ మరియు ఇతరులు., 1982; స్కోఫీల్డ్ 1982). మూడవ HMGCS2-స్వతంత్ర యంత్రాంగం d-?OHBని అమినో యాసిడ్ క్యాటాబోలిజం ద్వారా ఉత్పత్తి చేస్తుంది, ముఖ్యంగా లూసిన్ మరియు లైసిన్. నాల్గవ మెకానిజం స్పష్టంగా కనిపిస్తుంది ఎందుకంటే ఇది లేబులింగ్ ఆర్టిఫ్యాక్ట్ కారణంగా ఉంది మరియు దీనిని సూడోకెటోజెనిసిస్ అని పిలుస్తారు. ఈ దృగ్విషయం SCOT మరియు థియోలేస్ ప్రతిచర్యల యొక్క రివర్సిబిలిటీకి ఆపాదించబడింది మరియు ఎక్స్ట్రాహెపాటిక్ కణజాలంలో కీటోన్ బాడీ ట్రేసర్ యొక్క ఐసోటోపిక్ పలుచన కారణంగా కీటోన్ బాడీ టర్నోవర్ను ఎక్కువగా అంచనా వేయవచ్చు (డెస్ రోసియర్స్ మరియు ఇతరులు, 1990; ఫింక్ మరియు ఇతరులు., 1988). . అయినప్పటికీ, సూడోకెటోజెనిసిస్ చాలా సందర్భాలలో చాలా తక్కువగా ఉండవచ్చు (బెయిలీ మరియు ఇతరులు, 1990; కెల్లర్ మరియు ఇతరులు., 1978). ఒక స్కీమాటిక్ (Fig. 2A) కీటోన్ల యొక్క ఎలివేటెడ్ కణజాల స్థిరమైన స్థితిని పరిగణనలోకి తీసుకునేటప్పుడు దరఖాస్తు చేయడానికి ఉపయోగకరమైన విధానాన్ని సూచిస్తుంది.
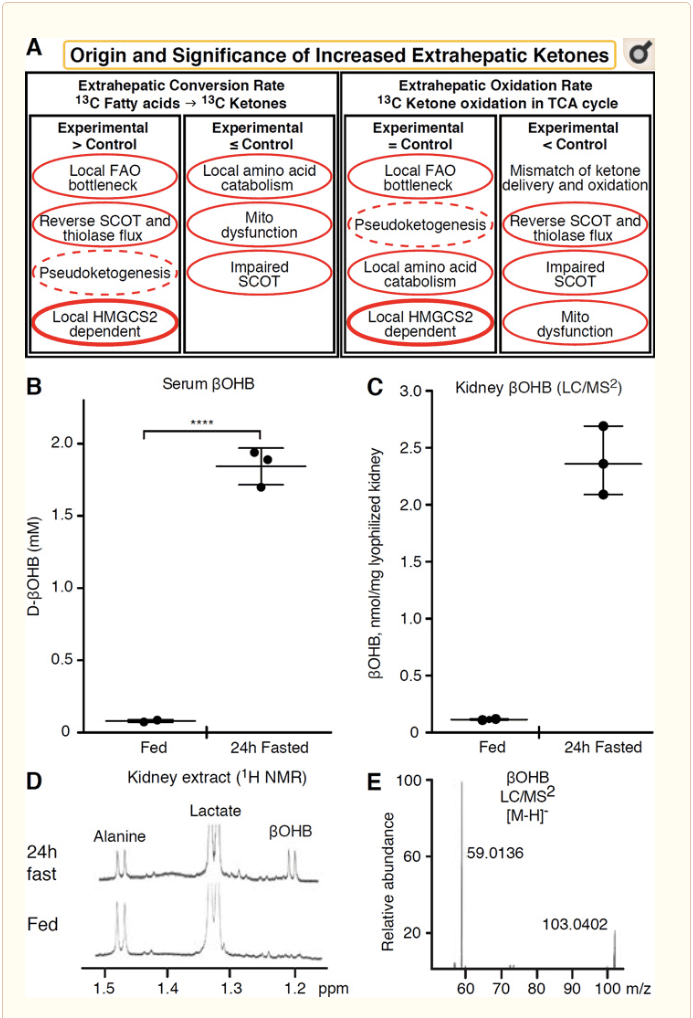

కిడ్నీ ఇటీవల కెటోజెనిక్ అవయవంగా దృష్టిని ఆకర్షించింది. చాలా రాష్ట్రాలలో, మూత్రపిండాలు కాలేయం-ఉత్పన్నమైన కీటోన్ బాడీల నికర వినియోగదారు, రక్తప్రవాహం నుండి కీటోన్ శరీరాలను విసర్జించడం లేదా తిరిగి గ్రహించడం, మరియు మూత్రపిండాలు సాధారణంగా నెట్ కీటోన్ బాడీ జనరేటర్ లేదా కాన్సంట్రేటర్ కాదు (రాబిన్సన్ మరియు విలియమ్సన్, 1980). ఒక కృత్రిమ ప్రయోగాత్మక వ్యవస్థలో లెక్కించబడిన కనిష్ట మూత్రపిండ కీటోజెనిసిస్ శారీరకంగా సంబంధితంగా లేదని శాస్త్రీయ అధ్యయనం యొక్క రచయితలు నిర్ధారించారు (వీడెమాన్ మరియు క్రెబ్స్, 1969). ఇటీవల, మూత్రపిండ కీటోజెనిసిస్ డయాబెటిక్ మరియు ఆటోఫాగి లోపం ఉన్న మౌస్ మోడల్లలో ఊహించబడింది, అయితే మెటబాలిక్ హోమియోస్టాసిస్లో బహుళ-అవయవ మార్పులు బహుళ అవయవాలపై ఇన్పుట్ల ద్వారా ఇంటిగ్రేటివ్ కీటోన్ జీవక్రియను మార్చే అవకాశం ఉంది (తకాగి మరియు ఇతరులు, 2016a; Takagi etal. 2016b; జాంగ్ మరియు ఇతరులు., 2011). ఒక ఇటీవలి ప్రచురణ మూత్రపిండాలలో ఇస్కీమియా-రిపెర్ఫ్యూజన్ గాయానికి వ్యతిరేకంగా రక్షిత యంత్రాంగంగా మూత్రపిండ కీటోజెనిసిస్ను సూచించింది (ట్రాన్ మరియు ఇతరులు, 2016). ఎలుకల మూత్రపిండ కణజాల సారాల నుండి ?OHB యొక్క సంపూర్ణ స్థిరమైన స్థితి సాంద్రతలు ~4–12 mM వద్ద నివేదించబడ్డాయి. ఇది సహేతుకమైనదో కాదో పరీక్షించడానికి, మేము తినిపించిన మరియు 24 గంటలు ఉపవాసం ఉన్న ఎలుకల నుండి మూత్రపిండ సారాలలో ?OHB సాంద్రతలను లెక్కించాము. రక్తరసి ?OHB సాంద్రతలు 100h ఉపవాసంతో ~2 ~M నుండి 24 mMకి పెరిగాయి (Fig. 2B), అయితే మూత్రపిండ స్థిరమైన స్థితి ?OHB సాంద్రతలు తినిపించిన స్థితిలో సుమారు 100 μM మరియు 1h ఉపవాస స్థితిలో 24 mM మాత్రమే (Fig. 2C'E), 45 సంవత్సరాల క్రితం లెక్కించబడిన ఏకాగ్రతలకు అనుగుణంగా ఉండే పరిశీలనలు (హెమ్స్ మరియు బ్రాస్నన్, 1970). కీటోటిక్ స్థితులలో, కాలేయం-ఉత్పన్నమైన కీటోన్ శరీరాలు రెనోప్రొటెక్టివ్గా ఉండే అవకాశం ఉంది, అయితే మూత్రపిండ కీటోజెనిసిస్కు రుజువు మరింత రుజువు అవసరం. నిజమైన ఎక్స్ట్రాహెపాటిక్ కీటోజెనిసిస్కు మద్దతు ఇచ్చే బలవంతపు సాక్ష్యం RPEలో సమర్పించబడింది (అడిజాంటో మరియు ఇతరులు., 2014). ఈ చమత్కారమైన జీవక్రియ పరివర్తన RPE-ఉత్పన్నమైన కీటోన్లను ఫోటోరిసెప్టర్ లేదా M'ller glia కణాలకు ప్రవహించేలా అనుమతించాలని సూచించబడింది, ఇది ఫోటోరిసెప్టర్ బాహ్య విభాగం యొక్క పునరుత్పత్తికి సహాయపడుతుంది.
?OHB సిగ్నలింగ్ మధ్యవర్తిగా
అవి శక్తివంతంగా సంపన్నమైనవి అయినప్పటికీ, కీటోన్ శరీరాలు సెల్యులార్ హోమియోస్టాసిస్లో రెచ్చగొట్టే "నాన్-కానానికల్" సిగ్నలింగ్ పాత్రలను ప్రదర్శిస్తాయి (Fig. 3) (న్యూమాన్ మరియు వెర్డిన్, 2014; రోజాస్-మోరేల్స్ మరియు ఇతరులు., 2016). ఉదాహరణకు, ?OHB క్లాస్ I HDACలను నిరోధిస్తుంది, ఇది హిస్టోన్ ఎసిటైలేషన్ను పెంచుతుంది మరియు తద్వారా ఆక్సీకరణ ఒత్తిడిని తగ్గించే జన్యువుల వ్యక్తీకరణను ప్రేరేపిస్తుంది (షిమాజు మరియు ఇతరులు., 2013). ?OHB అనేది ఉపవాసం లేదా స్ట్రెప్టోజోటోసిన్ ప్రేరిత డయాబెటిక్ ఎలుకల (Xie మరియు ఇతరులు, 2016) కాలేయాలలో లైసిన్ అవశేషాల వద్ద హిస్టోన్ కోవాలెంట్ మాడిఫైయర్ (క్రింద కూడా చూడండి, కీటోన్ బాడీ మెటబాలిజం యొక్క ఏకీకరణ, పోస్ట్-ట్రాన్స్లేషనల్ మోడిఫికేషన్, మరియు సెల్ కీటోన్ బాడీలు, ఆక్సీకరణ ఒత్తిడి మరియు న్యూరోప్రొటెక్షన్).
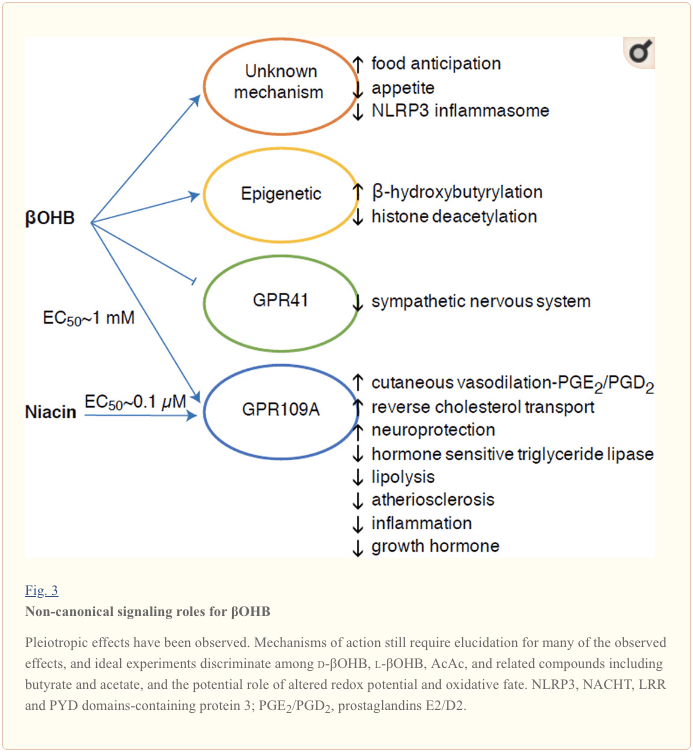
?OHB కూడా G-ప్రోటీన్ కపుల్డ్ గ్రాహకాల ద్వారా ప్రభావవంతంగా ఉంటుంది. అస్పష్టమైన మాలిక్యులర్ మెకానిజమ్స్ ద్వారా, ఇది సానుభూతిగల నాడీ వ్యవస్థ కార్యకలాపాలను అణిచివేస్తుంది మరియు G ప్రోటీన్ కపుల్డ్ రిసెప్టర్ 41 (GPR41) (కిమురా మరియు ఇతరులు, 2011) ద్వారా షార్ట్ చైన్ ఫ్యాటీ యాసిడ్ సిగ్నలింగ్ను నిరోధించడం ద్వారా మొత్తం శక్తి వ్యయం మరియు హృదయ స్పందన రేటును తగ్గిస్తుంది. ?OHB అనేది GPR109A (HCAR2 అని కూడా పిలుస్తారు), కొవ్వు కణజాలాలలో (తెలుపు మరియు గోధుమ) వ్యక్తీకరించబడిన GPCR ఉప-కుటుంబ సభ్యుడు (తునారు మరియు ఇతరులు, 2003) మరియు రోగనిరోధక కణాలు (అహ్మద్ మరియు ఇతరులు, 2009). ?OHB అనేది d-?OHB, l-?OHB, మరియు బ్యూటిరేట్ ద్వారా సక్రియం చేయబడిన GPR109A రిసెప్టర్ (EC50 ~770 ~M) యొక్క ఏకైక అంతర్జాత లిగాండ్, కానీ AcAc కాదు (Taggart et al., 2005). GPR109A యాక్టివేషన్ కోసం అధిక సాంద్రత థ్రెషోల్డ్ కీటోజెనిక్ డైట్, ఆకలితో లేదా కీటోయాసిడోసిస్ సమయంలో కట్టుబడి ఉండటం ద్వారా సాధించబడుతుంది, ఇది కొవ్వు కణజాల లిపోలిసిస్ నిరోధానికి దారితీస్తుంది. GPR109A యొక్క యాంటీ-లిపోలిటిక్ ప్రభావం అడెనైల్ సైక్లేస్ను నిరోధించడం మరియు cAMP తగ్గడం, హార్మోన్ సెన్సిటివ్ ట్రైగ్లిజరైడ్ లైపేస్ను నిరోధించడం ద్వారా కొనసాగుతుంది (అహ్మద్ మరియు ఇతరులు, 2009; తునారు మరియు ఇతరులు., 2003). ఇది ప్రతికూల ఫీడ్బ్యాక్ లూప్ను సృష్టిస్తుంది, దీనిలో కీటోసిస్ అడిపోసైట్ల నుండి ఎస్టెరిఫైడ్ కాని కొవ్వు ఆమ్లాల విడుదలను తగ్గించడం ద్వారా కీటోజెనిసిస్పై మాడ్యులేటరీ బ్రేక్ను ఉంచుతుంది (అహ్మద్ మరియు ఇతరులు, 2009; టాగ్గార్ట్ మరియు ఇతరులు., 2005), దీని ప్రభావం ద్వారా సమతుల్యం చేయవచ్చు. లిపోలిసిస్ను ప్రేరేపించే సానుభూతి డ్రైవ్. నియాసిన్ (విటమిన్ B3, నికోటినిక్ యాసిడ్) అనేది GRP50A కోసం ఒక శక్తివంతమైన (EC0.1 ~ 109 ~M) లిగాండ్, ఇది డైస్లిపిడెమియాలకు దశాబ్దాలుగా సమర్థవంతంగా ఉపయోగించబడుతుంది (బెన్యో మరియు ఇతరులు, 2005; బెన్యో మరియు ఇతరులు., 2006; 2010al. లుకాసోవా మరియు ఇతరులు., 2011; తునారు మరియు ఇతరులు., 2003). నియాసిన్ మాక్రోఫేజ్లలో రివర్స్ కొలెస్ట్రాల్ రవాణాను మెరుగుపరుస్తుంది మరియు అథెరోస్క్లెరోటిక్ గాయాలను తగ్గిస్తుంది (లుకాసోవా మరియు ఇతరులు., 2011), అథెరోస్క్లెరోటిక్ గాయాలపై ?OHB యొక్క ప్రభావాలు తెలియవు. GPR109A గ్రాహకం రక్షిత పాత్రలను కలిగి ఉన్నప్పటికీ, స్ట్రోక్ మరియు న్యూరోడెజెనరేటివ్ వ్యాధులలో కీటోజెనిక్ డైట్ వాడకం మధ్య చమత్కారమైన కనెక్షన్లు ఉన్నప్పటికీ (Fu et al., 2015; Rahman et al., 2014), GPR109A ద్వారా ?OHB యొక్క రక్షిత పాత్ర వివో విధ్వంసం కాలేదు. .
చివరగా, ?OHB ఆకలి మరియు సంతృప్తిని ప్రభావితం చేయవచ్చు. కీటోజెనిక్ మరియు చాలా తక్కువ శక్తి ఆహారాల ప్రభావాలను కొలిచిన అధ్యయనాల యొక్క మెటా-విశ్లేషణ నియంత్రణ ఆహారాలతో పోలిస్తే, ఈ ఆహారాలను తీసుకునే పాల్గొనేవారు అధిక సంతృప్తిని ప్రదర్శిస్తారని నిర్ధారించారు (గిబ్సన్ మరియు ఇతరులు., 2015). అయినప్పటికీ, ఆకలిని మాడ్యులేట్ చేసే అదనపు జీవక్రియ లేదా హార్మోన్ల మూలకాలు ఈ ప్రభావానికి ఆమోదయోగ్యమైన వివరణ. ఉదాహరణకు, ఎలుకల కీటోజెనిక్ డైట్లో నిర్వహించబడే ఎలుకలు చౌ కంట్రోల్-ఫెడ్ ఎలుకలతో పోలిస్తే పెరిగిన శక్తి వ్యయాన్ని ప్రదర్శించాయి, అదే విధమైన కేలరీలు తీసుకున్నప్పటికీ, లెప్టిన్ లేదా పెప్టైడ్ల జన్యువులను ప్రసరించడంలో మార్పు లేదు (కెన్నెడీ మరియు ఇతరులు, 2007). ?OHB ద్వారా ఆకలిని అణచివేయడాన్ని సూచించే ప్రతిపాదిత మెకానిజమ్లలో సిగ్నలింగ్ మరియు ఆక్సీకరణ రెండూ ఉన్నాయి (Laeger et al., 2010). సిర్కాడియన్ రిథమ్ జీన్ (Per2) యొక్క హెపాటోసైట్ నిర్దిష్ట తొలగింపు మరియు క్రోమాటిన్ ఇమ్యునోప్రెసిపిటేషన్ అధ్యయనాలు PER2 నేరుగా Cpt1a జన్యువును సక్రియం చేస్తుందని మరియు Hmgcs2ని పరోక్షంగా నియంత్రిస్తుంది, ఇది Per2 నాకౌట్ ఎలుకలలో బలహీనమైన కీటోసిస్కు దారితీస్తుందని వెల్లడించింది (చావన్ 2016, ఇతరులు). ఈ ఎలుకలు బలహీనమైన ఆహార నిరీక్షణను ప్రదర్శించాయి, ఇది దైహిక ?OHB పరిపాలన ద్వారా పాక్షికంగా పునరుద్ధరించబడింది. కేంద్ర నాడీ వ్యవస్థను ప్రత్యక్ష ?OHB లక్ష్యంగా నిర్ధారించడానికి భవిష్యత్తు అధ్యయనాలు అవసరం మరియు గమనించిన ప్రభావాలకు కీటోన్ ఆక్సీకరణ అవసరమా లేదా మరొక సిగ్నలింగ్ మెకానిజం ప్రమేయం ఉందా. ఇతర పరిశోధకులు ఆహారం తీసుకోవడం యొక్క నియంత్రకంగా వెంట్రోమీడియల్ హైపోథాలమస్లోని స్థానిక ఆస్ట్రోసైట్-ఉత్పన్నమైన కీటోజెనిసిస్ యొక్క అవకాశాన్ని ఉపయోగించారు, అయితే ఈ ప్రాథమిక పరిశీలనలు జన్యు మరియు ఫ్లక్స్-ఆధారిత అంచనాల నుండి కూడా ప్రయోజనం పొందుతాయి (లే ఫోల్ మరియు ఇతరులు., 2014). విఫలమైన బరువు తగ్గించే ప్రయత్నాలలో ఆకలి మరియు తృప్తి ముఖ్యమైన అంశాలు కాబట్టి కీటోసిస్ మరియు పోషకాల లేమి మధ్య సంబంధం ఆసక్తిని కలిగి ఉంది.
కీటోన్ బాడీ మెటబాలిజం, పోస్ట్-ట్రాన్స్లేషనల్ మోడిఫికేషన్ మరియు సెల్ ఫిజియాలజీ యొక్క ఏకీకరణ
కీటోన్ బాడీలు అసిటైల్-CoA యొక్క కంపార్ట్మెంటలైజ్డ్ పూల్స్కు దోహదం చేస్తాయి, ఇది సెల్యులార్ జీవక్రియలో ప్రముఖ పాత్రలను ప్రదర్శించే కీలకమైన ఇంటర్మీడియట్ (పియట్రోకోలా మరియు ఇతరులు., 2015). ఎసిటైల్-CoA యొక్క ఒక పాత్ర ఏమిటంటే, ఎసిటైలేషన్కు సబ్స్ట్రేట్గా పనిచేయడం, ఇది ఎంజైమ్గా-ఉత్ప్రేరక హిస్టోన్ సమయోజనీయ మార్పు (చౌదరి మరియు ఇతరులు, 2014; దత్తా మరియు ఇతరులు., 2016; ఫ్యాన్ మరియు ఇతరులు., 2015; మెన్జీస్ మరియు ఇతరులు. ) పెద్ద సంఖ్యలో డైనమిక్గా ఎసిటైలేటెడ్ మైటోకాన్డ్రియల్ ప్రోటీన్లు, వీటిలో చాలా వరకు నాన్-ఎంజైమాటిక్ మెకానిజమ్స్ ద్వారా సంభవించవచ్చు, గణన ప్రోటీమిక్స్ అధ్యయనాల నుండి కూడా ఉద్భవించాయి (డిట్టెన్హాఫర్-రీడ్ మరియు ఇతరులు., 2016; హెబర్ట్ మరియు ఇతరులు., 2015; రార్డిన్ మరియు ఇతరులు. ; షిమాజు మరియు ఇతరులు., 2013). లైసిన్ డీసిటైలేస్లు జింక్ కోఫాక్టర్ (ఉదా, న్యూక్లియోసైటోసోలిక్ HDACలు) లేదా NAD+ని సహ-సబ్స్ట్రేట్గా (సిర్టుయిన్లు, SIRTలు) ఉపయోగిస్తాయి (చౌదరి మరియు ఇతరులు, 2013; మెన్జీస్ మరియు ఇతరులు., 2010). ఎసిటైల్ప్రొటీమ్ మొత్తం సెల్యులార్ ఎసిటైల్-CoA పూల్ యొక్క సెన్సార్ మరియు ఎఫెక్టార్గా పనిచేస్తుంది, ఎందుకంటే ఫిజియోలాజికల్ మరియు జెనెటిక్ మానిప్యులేషన్లు ప్రతి ఒక్కటి ఎసిటైలేషన్ యొక్క ఎంజైమాటిక్ కాని ప్రపంచ వైవిధ్యాలకు దారితీస్తాయి (వీనర్ట్ మరియు ఇతరులు., 2014). కణాంతర జీవక్రియలు లైసిన్ అవశేష ఎసిటైలేషన్ యొక్క మాడ్యులేటర్లుగా పనిచేస్తాయి కాబట్టి, కీటోన్ బాడీల పాత్రను పరిగణనలోకి తీసుకోవడం చాలా ముఖ్యం, దీని సమృద్ధి అత్యంత డైనమిక్.
?OHB అనేది కనీసం రెండు మెకానిజమ్స్ ద్వారా ఎపిజెనెటిక్ మాడిఫైయర్. పెరిగిన ?OHB స్థాయిలు ఉపవాసం, కేలరీల పరిమితి, డైరెక్ట్ అడ్మినిస్ట్రేషన్ లేదా సుదీర్ఘమైన వ్యాయామం HDAC నిరోధం లేదా హిస్టోన్ ఎసిటైల్ట్రాన్స్ఫేరేస్ యాక్టివేషన్ను రేకెత్తిస్తాయి (మరోసి మరియు ఇతరులు, 2016; స్లీమాన్ మరియు ఇతరులు., 2016) లేదా ఆక్సీకరణ ఒత్తిడికి (షిమజ్యుయేషన్, 2013.) . ?HDAC3 యొక్క OHB నిరోధం నవజాత జీవక్రియ శరీరధర్మ శాస్త్రాన్ని నియంత్రించగలదు (రాండో మరియు ఇతరులు., 2016). స్వతంత్రంగా, ?OHB నేరుగా హిస్టోన్ లైసిన్ అవశేషాలను సవరించింది (Xie et al., 2016). సుదీర్ఘ ఉపవాసం, లేదా స్టెప్టోజోటోసిన్-ప్రేరిత డయాబెటిక్ కీటోయాసిడోసిస్ హిస్టోన్ ?-హైడ్రాక్సీబ్యూటైరిలేషన్ను పెంచింది. లైసిన్ ?-హైడ్రాక్సీబ్యూటైరిలేషన్ మరియు ఎసిటైలేషన్ సైట్ల సంఖ్య పోల్చదగినది అయినప్పటికీ, ఎసిటైలేషన్ కంటే స్టోయికియోమెట్రిక్గా ఎక్కువ హిస్టోన్?-హైడ్రాక్సీబ్యూటైరిలేషన్ గమనించబడింది. విభిన్న జన్యువులు హిస్టోన్ లైసిన్ ?-హైడ్రాక్సీబ్యూటైరిలేషన్, వర్సెస్ ఎసిటైలేషన్ లేదా మిథైలేషన్ ద్వారా ప్రభావితమయ్యాయి, ఇది విభిన్న సెల్యులార్ ఫంక్షన్లను సూచిస్తుంది. ?-హైడ్రాక్సీబ్యూటైరిలేషన్ అనేది ఆకస్మికమా లేదా ఎంజైమాటిక్ అనేది తెలియదు, అయితే కీటోన్ బాడీల ద్వారా మెకానిజమ్ల పరిధిని విస్తరిస్తుంది, ట్రాన్స్క్రిప్షన్ను డైనమిక్గా ప్రభావితం చేస్తుంది.
కేలరీల పరిమితి మరియు పోషకాల కొరత సమయంలో అవసరమైన సెల్ రిప్రోగ్రామింగ్ సంఘటనలు వరుసగా SIRT3- మరియు SIRT5-ఆధారిత మైటోకాన్డ్రియల్ డీసీటైలేషన్ మరియు డీసుసినిలేషన్లో మధ్యవర్తిత్వం వహించవచ్చు, కాలేయం మరియు ఎక్స్ట్రాహెపాటిక్ కణజాలాలలో అనువదించిన తర్వాత స్థాయిలో కీటోజెనిక్ మరియు కీటోలైటిక్ ప్రోటీన్లను నియంత్రిస్తుంది. 2015; హెబర్ట్ మరియు ఇతరులు., 2013; రార్డిన్ మరియు ఇతరులు., 2013; షిమాజు మరియు ఇతరులు., 2010). ఆక్రమిత సైట్ల యొక్క స్టోయికియోమెట్రిక్ పోలిక తప్పనిసరిగా జీవక్రియ ఫ్లక్స్లో మార్పులకు నేరుగా లింక్ చేయనప్పటికీ, మైటోకాన్డ్రియల్ ఎసిటైలేషన్ డైనమిక్ మరియు ఎంజైమాటిక్ ఎసిటైల్ట్రాన్స్ఫేరేసెస్ (వాగ్నెర్సెస్ మరియు 2013) కంటే ఎసిటైల్-CoA గాఢత లేదా మైటోకాన్డ్రియల్ pH ద్వారా నడపబడుతుంది. కీటోన్ బాడీ మెటబోలైజింగ్ ఎంజైమ్ల యొక్క SIRT3 మరియు SIRT5 మాడ్యులేట్ కార్యకలాపాలు అసిటైల్ప్రొటీమ్, సక్సినైల్ప్రోటీమ్ మరియు ఇతర డైనమిక్ సెల్యులార్ లక్ష్యాలను చెక్కడంలో కీటోన్ల పరస్పర పాత్ర గురించి ప్రశ్నను రేకెత్తిస్తాయి. నిజానికి, కీటోజెనిసిస్ యొక్క వైవిధ్యాలు NAD+ సాంద్రతలను ప్రతిబింబిస్తాయి కాబట్టి, కీటోన్ ఉత్పత్తి మరియు సమృద్ధి sirtuin కార్యాచరణను నియంత్రిస్తుంది, తద్వారా మొత్తం ఎసిటైల్-CoA/succinyl-CoA పూల్స్, ఎసిల్ప్రొటీమ్ మరియు మైటోకాన్డ్రియల్ మరియు సెల్ ఫిజియాలజీని ప్రభావితం చేస్తుంది. ?-ఎంజైమ్ లైసిన్ అవశేషాల హైడ్రాక్సీబ్యూటైరిలేషన్ సెల్యులార్ రీప్రొగ్రామింగ్కు మరొక పొరను జోడించగలదు. ఎక్స్ట్రాహెపాటిక్ కణజాలాలలో, కీటోన్ బాడీ ఆక్సీకరణ సెల్ హోమియోస్టాసిస్లో సారూప్య మార్పులను ప్రేరేపిస్తుంది. ఎసిటైల్-CoA పూల్స్ యొక్క కంపార్ట్మెంటేషన్ అత్యంత నియంత్రించబడి, సెల్యులార్ మార్పుల యొక్క విస్తృత వర్ణపటాన్ని సమన్వయం చేస్తుంది, మైటోకాన్డ్రియల్ మరియు సైటోప్లాస్మిక్ ఎసిటైల్-CoA సాంద్రతలు రెండింటినీ నేరుగా ఆకృతి చేసే కీటోన్ బాడీల సామర్థ్యానికి స్పష్టత అవసరం (చెన్ మరియు ఇతరులు, 2012; కార్బెట్. 2016; పౌగోవ్కినా మరియు ఇతరులు., 2014; ష్వెర్ మరియు ఇతరులు., 2009; వెల్లన్ మరియు థాంప్సన్, 2012). ఎసిటైల్-CoA సాంద్రతలు కఠినంగా నియంత్రించబడతాయి మరియు ఎసిటైల్-CoA పొర అంతర్లీనంగా ఉన్నందున, TCA చక్రంలో ఉత్పత్తి మరియు టెర్మినల్ ఆక్సీకరణ రేట్లు, కీటోన్డ్రియల్ బాడీలుగా మార్చడం, ఎసిటైల్-CoA హోమియోస్టాసిస్ను సమన్వయం చేసే డ్రైవర్ మెకానిజమ్లను పరిగణనలోకి తీసుకోవడం చాలా ముఖ్యం. కార్నిటైన్ ఎసిటైల్ట్రాన్స్ఫేరేస్ (CrAT) ద్వారా ప్రసరించడం లేదా సిట్రేట్గా మార్చబడిన తర్వాత సైటోసోల్కు ఎసిటైల్-CoA ఎగుమతి మరియు ATP సిట్రేట్ లైస్ (ACLY) ద్వారా విడుదల అవుతుంది. సెల్ ఎసిటైల్ప్రొటీమ్ మరియు హోమియోస్టాసిస్లో ఈ తరువాతి మెకానిజమ్ల యొక్క ముఖ్య పాత్రలకు కీటోజెనిసిస్ మరియు కీటోన్ ఆక్సీకరణ పాత్రల గురించి సరిపోలిన అవగాహన అవసరం (దాస్ మరియు ఇతరులు, 2015; మెక్డొన్నెల్ మరియు ఇతరులు., 2016; మౌసైఫ్ మరియు ఇతరులు., 2015; 2015; సెయిలర్ మరియు ఇతరులు., 2014; సెయిలర్ మరియు ఇతరులు., 2015; వెల్లన్ మరియు ఇతరులు., 2009; వెల్లన్ మరియు థాంప్సన్, 2012). లక్ష్యాలు మరియు ఫలితాలను పేర్కొనడానికి జన్యుపరంగా తారుమారు చేయబడిన నమూనాల అమరికలో జీవక్రియ మరియు ఎసిల్ప్రొటోమిక్స్లో కన్వర్జెంట్ టెక్నాలజీలు అవసరం.
కీటోన్ బాడీస్కు యాంటీ మరియు ప్రో-ఇన్ఫ్లమేటరీ రెస్పాన్స్
కీటోసిస్ మరియు కీటోన్ బాడీలు వాపు మరియు రోగనిరోధక కణాల పనితీరును మాడ్యులేట్ చేస్తాయి, అయితే వైవిధ్యమైన మరియు వ్యత్యాస విధానాలు కూడా ప్రతిపాదించబడ్డాయి. దీర్ఘకాలిక పోషకాహార లేమి మంటను తగ్గిస్తుంది (యుమ్ మరియు ఇతరులు, 2015), అయితే టైప్ 1 మధుమేహం యొక్క దీర్ఘకాలిక కీటోసిస్ అనేది శోథ నిరోధక స్థితి (జైన్ మరియు ఇతరులు, 2002; కనికర్లా-మేరీ మరియు జైన్, 2015; కురేపా మరియు ఇతరులు., 2012 ) మంటలో ?OHB కోసం మెకానిజం-ఆధారిత సిగ్నలింగ్ పాత్రలు ఉద్భవించాయి ఎందుకంటే మాక్రోఫేజ్లు లేదా మోనోసైట్లతో సహా అనేక రోగనిరోధక వ్యవస్థ కణాలు GPR109Aను సమృద్ధిగా వ్యక్తీకరిస్తాయి. ?OHB ప్రధానంగా యాంటీ ఇన్ఫ్లమేటరీ రెస్పాన్స్ను (Fu et al., 2014; గంభీర్ et al., 2012; Rahman et al., 2014; Youm et al., 2015), కీటోన్ బాడీల అధిక సాంద్రతలు, ముఖ్యంగా AcAC, మే ప్రో-ఇన్ఫ్లమేటరీ ప్రతిస్పందనను ట్రిగ్గర్ చేయండి (జైన్ మరియు ఇతరులు, 2002; కనికర్ల-మేరీ మరియు జైన్, 2015; కురేపా మరియు ఇతరులు., 2012).
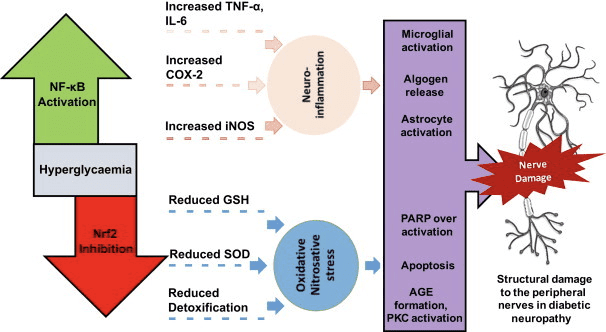
అథెరోస్క్లెరోసిస్, స్థూలకాయం, తాపజనక ప్రేగు వ్యాధి, నాడీ సంబంధిత వ్యాధి మరియు క్యాన్సర్లో GPR109A లిగాండ్ల యొక్క యాంటీ ఇన్ఫ్లమేటరీ పాత్రలు సమీక్షించబడ్డాయి (గ్రాఫ్ మరియు ఇతరులు., 2016). GPR109A వ్యక్తీకరణ డయాబెటిక్ మోడల్స్, హ్యూమన్ డయాబెటిక్ రోగులు (గంభీర్ మరియు ఇతరులు, 2012) యొక్క RPE కణాలలో మరియు న్యూరోడెజెనరేషన్ సమయంలో మైక్రోగ్లియాలో (ఫు మరియు ఇతరులు, 2014) వృద్ధి చెందింది. ?OHB యొక్క యాంటీ ఇన్ఫ్లమేటరీ ఎఫెక్ట్స్ RPE కణాలలో GPR109A ఓవర్ ఎక్స్ప్రెషన్ ద్వారా మెరుగుపరచబడ్డాయి మరియు GPR109A యొక్క ఫార్మకోలాజికల్ ఇన్హిబిషన్ లేదా జెనెటిక్ నాకౌట్ ద్వారా రద్దు చేయబడ్డాయి (గంభీర్ మరియు ఇతరులు., 2012). ?OHB మరియు ఎక్సోజనస్ నికోటినిక్ యాసిడ్ (Taggart et al., 2005), రెండూ TNFలో యాంటీ ఇన్ఫ్లమేటరీ ఎఫెక్ట్లను అందజేస్తాయా? లేదా ప్రో-ఇన్ఫ్లమేటరీ ప్రొటీన్ల (iNOS, COX-2), లేదా స్రవించే సైటోకిన్లు (TNF?, IL-1?, IL-6, CCL2/MCP-1) స్థాయిలను తగ్గించడం ద్వారా LPS-ప్రేరిత వాపు, కొంతవరకు NFని నిరోధించడం ద్వారా -?B ట్రాన్స్లోకేషన్ (ఫు మరియు ఇతరులు, 2014; గంభీర్ మరియు ఇతరులు., 2012). ?OHB ER ఒత్తిడిని తగ్గిస్తుంది మరియు NLRP3 ఇన్ఫ్లమేసమ్, యాంటీఆక్సిడేటివ్ స్ట్రెస్ రెస్పాన్స్ని యాక్టివేట్ చేస్తుంది (బే మరియు ఇతరులు, 2016; యూమ్ మరియు ఇతరులు., 2015). అయినప్పటికీ, న్యూరోడెజెనరేటివ్ ఇన్ఫ్లమేషన్లో, GPR109A-ఆధారిత ?OHB-మెడియేటెడ్ ప్రొటెక్షన్లో MAPK పాత్వే సిగ్నలింగ్ (ఉదా, ERK, JNK, p38) (Fu et al., 2014) వంటి ఇన్ఫ్లమేటరీ మధ్యవర్తులు ఉండరు, కానీ COX-1-ఆధారిత PGD2 అవసరం కావచ్చు ఉత్పత్తి (రెహ్మాన్ మరియు ఇతరులు, 2014). ఇస్కీమిక్ స్ట్రోక్ మోడల్లో (రెహ్మాన్ మరియు ఇతరులు, 109) న్యూరోప్రొటెక్టివ్ ప్రభావాన్ని చూపడానికి మాక్రోఫేజ్ GPR2014A అవసరమని ఆశ్చర్యంగా ఉంది, అయితే ఎముక మజ్జలో NLRP3 ఇన్ఫ్లమేసమ్ను నిరోధించడానికి ?OHB సామర్థ్యం స్వతంత్రంగా ఉంటుంది (మాక్రోఫేజెస్ GPR109A స్వతంత్రంగా ఉంటుంది. ., 2015). చాలా అధ్యయనాలు ?OHBని యాంటీ ఇన్ఫ్లమేటరీ ఎఫెక్ట్లకు లింక్ చేసినప్పటికీ, ?OHB ప్రో-ఇన్ఫ్లమేటరీ కావచ్చు మరియు దూడ హెపటోసైట్లలో లిపిడ్ పెరాక్సిడేషన్ యొక్క గుర్తులను పెంచుతుంది (షి మరియు ఇతరులు, 2014). ?OHB యొక్క యాంటీ-వర్సెస్ ప్రో-ఇన్ఫ్లమేటరీ ఎఫెక్ట్స్ సెల్ రకం, ?OHB ఏకాగ్రత, ఎక్స్పోజర్ వ్యవధి మరియు కో-మాడ్యులేటర్ల ఉనికి లేదా లేకపోవడంపై ఆధారపడి ఉండవచ్చు.
?OHB కాకుండా, AcAc ప్రో-ఇన్ఫ్లమేటరీ సిగ్నలింగ్ని సక్రియం చేయవచ్చు. ఎలివేటెడ్ AcAc, ముఖ్యంగా అధిక గ్లూకోజ్ సాంద్రతతో, NADPH ఆక్సిడేస్/ఆక్సిడేటివ్ స్ట్రెస్ డిపెండెంట్ మెకానిజం ద్వారా ఎండోథెలియల్ సెల్ గాయాన్ని తీవ్రతరం చేస్తుంది (కనికర్లా-మేరీ మరియు జైన్, 2015). డయాబెటిక్ తల్లుల బొడ్డు తాడులో అధిక AcAc సాంద్రతలు అధిక ప్రోటీన్ ఆక్సీకరణ రేటు మరియు MCP-1 గాఢతతో పరస్పర సంబంధం కలిగి ఉన్నాయి (కురేపా మరియు ఇతరులు., 2012). డయాబెటిక్ రోగులలో అధిక AcAc TNFతో పరస్పర సంబంధం కలిగి ఉందా? వ్యక్తీకరణ (జైన్ మరియు ఇతరులు, 2002), మరియు AcAc, కానీ ?OHB, ప్రేరేపిత TNF?, MCP-1 వ్యక్తీకరణ, ROS సంచితం మరియు U937 మానవ మోనోసైట్ కణాలలో cAMP స్థాయి తగ్గింది (జైన్ మరియు ఇతరులు, 2002; కురేపా మరియు ఇతరులు ., 2012).
కీటోన్ బాడీ డిపెండెంట్ సిగ్నలింగ్ దృగ్విషయాలు తరచుగా అధిక కీటోన్ బాడీ సాంద్రతలతో (> 5 mM) ప్రేరేపించబడతాయి మరియు అస్పష్టమైన యంత్రాంగాల ద్వారా కీటోన్లను ప్రో- లేదా యాంటీ ఇన్ఫ్లమేటరీ ప్రభావాలకు అనుసంధానించే అనేక అధ్యయనాల విషయంలో. అదనంగా, మంటపై ?OHB వర్సెస్ AcAc యొక్క విరుద్ధమైన ప్రభావాలు మరియు మైటోకాన్డ్రియల్ రెడాక్స్ సంభావ్యతను ప్రభావితం చేసే AcAc/?OHB నిష్పత్తి యొక్క సామర్థ్యం కారణంగా, సెల్యులార్ ఫినోటైప్లపై కీటోన్ బాడీల పాత్రలను అంచనా వేసే అత్యుత్తమ ప్రయోగాలు AcAc మరియు ? OHB వివిధ నిష్పత్తులలో మరియు వివిధ సంచిత సాంద్రతలలో [ఉదా, (సైటో మరియు ఇతరులు, 2016)]. చివరగా, AcAcని వాణిజ్యపరంగా లిథియం ఉప్పుగా లేదా ఉపయోగించే ముందు బేస్ జలవిశ్లేషణ అవసరమయ్యే ఇథైల్ ఈస్టర్గా మాత్రమే కొనుగోలు చేయవచ్చు. లిథియం కేషన్ స్వతంత్రంగా సిగ్నల్ ట్రాన్స్డక్షన్ క్యాస్కేడ్లను ప్రేరేపిస్తుంది (మంజి మరియు ఇతరులు, 1995), మరియు AcAc అయాన్ లేబుల్. చివరగా, రేస్మిక్ d/l-?OHBని ఉపయోగించి చేసిన అధ్యయనాలు గందరగోళానికి గురవుతాయి, ఎందుకంటే d-?OHB స్టీరియో ఐసోమర్ మాత్రమే AcAcకి ఆక్సీకరణం చెందుతుంది, అయితే d-?OHB మరియు l-?OHBలు GPR109A ద్వారా ప్రతి సిగ్నల్ను NLRP3 ఇన్ఫ్లమేసమ్ను నిరోధించగలవు, మరియు లిపోజెనిక్ సబ్స్ట్రేట్లుగా పనిచేస్తాయి.
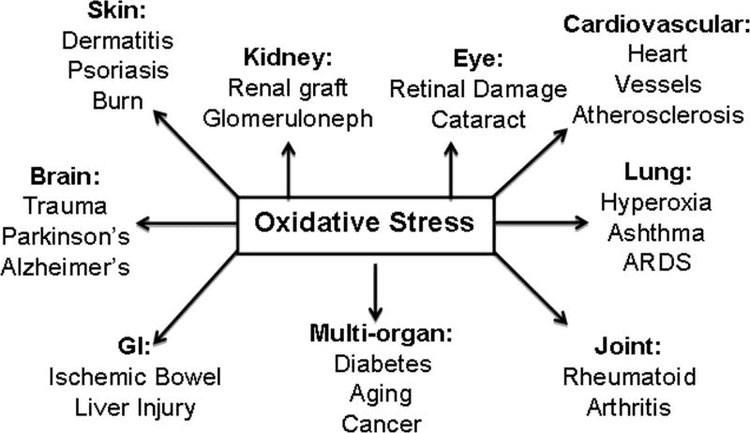
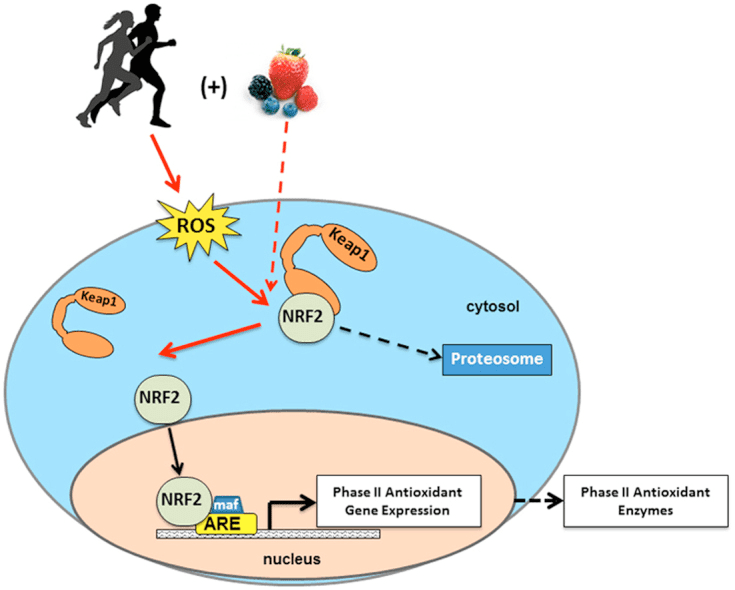
కీటోన్ బాడీస్, ఆక్సిడేటివ్ స్ట్రెస్ మరియు న్యూరోప్రొటెక్షన్
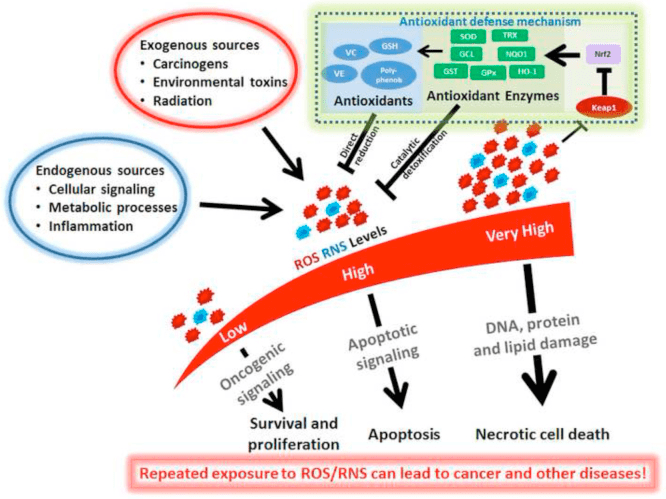
ఆక్సీకరణ ఒత్తిడి సాధారణంగా అధిక ఉత్పత్తి మరియు/లేదా బలహీనమైన తొలగింపు కారణంగా ROS అధికంగా ప్రదర్శించబడే స్థితిగా నిర్వచించబడుతుంది. కీటోన్ బాడీల యొక్క యాంటీఆక్సిడెంట్ మరియు ఆక్సీకరణ ఒత్తిడిని తగ్గించే పాత్రలు విట్రో మరియు వివోలో, ముఖ్యంగా న్యూరోప్రొటెక్షన్ సందర్భంలో విస్తృతంగా వివరించబడ్డాయి. చాలా న్యూరాన్లు కొవ్వు ఆమ్లాల నుండి అధిక-శక్తి ఫాస్ఫేట్లను ప్రభావవంతంగా ఉత్పత్తి చేయవు, కానీ కార్బోహైడ్రేట్లు తక్కువ సరఫరాలో ఉన్నప్పుడు కీటోన్ శరీరాలను ఆక్సీకరణం చేస్తాయి, కీటోన్ శరీరాల యొక్క న్యూరోప్రొటెక్టివ్ ప్రభావాలు చాలా ముఖ్యమైనవి (కాహిల్ GF Jr, 2006; ఎడ్మండ్ మరియు ఇతరులు., 1987; యాంగ్ మరియు ఇతరులు, 1987). ఆక్సీకరణ ఒత్తిడి నమూనాలలో, BDH1 ఇండక్షన్ మరియు SCOT అణచివేత వైవిధ్యమైన సెల్ సిగ్నలింగ్, రెడాక్స్ సంభావ్యత లేదా జీవక్రియ అవసరాలను కొనసాగించడానికి కీటోన్ బాడీ మెటబాలిజంను రీప్రోగ్రామ్ చేయవచ్చని సూచిస్తున్నాయి (నాగావో మరియు ఇతరులు, 2016; టియు మరియు ఇతరులు., 2003).
కీటోన్ బాడీలు న్యూరాన్లు మరియు కార్డియోమయోసైట్లలో సెల్యులార్ డ్యామేజ్, గాయం, మరణం మరియు తక్కువ అపోప్టోసిస్ యొక్క గ్రేడ్లను తగ్గిస్తాయి (హేసెస్ మరియు ఇతరులు, 2008; మలౌఫ్ మరియు ఇతరులు., 2007; నాగో మరియు ఇతరులు., 2016; టియు మరియు ఇతరులు., 2003). ప్రారంభించబడిన యంత్రాంగాలు వైవిధ్యంగా ఉంటాయి మరియు ఎల్లప్పుడూ ఏకాగ్రతకు సరళంగా సంబంధం కలిగి ఉండవు. (d లేదా l)-?OHB స్కావెంజ్ ROS (హైడ్రాక్సిల్ అయాన్) యొక్క తక్కువ మిల్లీమోలార్ సాంద్రతలు, అయితే AcAc అనేక ROS జాతులను స్కావెంజ్ చేస్తుంది, అయితే శారీరక పరిధిని (IC50 20–67 mM) మించిన సాంద్రతలలో మాత్రమే (Haces et al., 2008) . దీనికి విరుద్ధంగా, ఎలక్ట్రాన్ రవాణా గొలుసు యొక్క రెడాక్స్ సంభావ్యతపై ప్రయోజనకరమైన ప్రభావం సాధారణంగా d-?OHBకి అనుసంధానించబడిన ఒక యంత్రాంగం. మూడు కీటోన్ బాడీలు (d/l-?OHB మరియు AcAc) న్యూరానల్ సెల్ డెత్ మరియు ROS చేరడం గ్లైకోలిసిస్ యొక్క రసాయన నిరోధం ద్వారా ప్రేరేపించబడినప్పటికీ, d-?OHB మరియు AcAc మాత్రమే న్యూరానల్ ATP క్షీణతను నిరోధించాయి. దీనికి విరుద్ధంగా, హైపోగ్లైసీమిక్ ఇన్ వివో మోడల్లో, (d లేదా l)-?OHB, కానీ AcAc హిప్పోకాంపల్ లిపిడ్ పెరాక్సిడేషన్ను నిరోధించలేదు (హేసెస్ మరియు ఇతరులు, 2008; మలోఫ్ మరియు ఇతరులు., 2007; మరోసి మరియు ఇతరులు., 2016; మర్ఫీ, 2009; మర్ఫీ, ; టియు మరియు ఇతరులు., 2003). కీటోజెనిక్ ఆహారం (87% కిలో కేలరీలు కొవ్వు మరియు 13% ప్రోటీన్) తినిపించిన ఎలుకల యొక్క వివో అధ్యయనాలలో యాంటీఆక్సిడెంట్ సామర్థ్యం (జీగ్లర్ మరియు ఇతరులు, 2003) యొక్క న్యూరోఅనాటమికల్ వైవిధ్యాన్ని ప్రదర్శించారు, ఇక్కడ హిప్పోకాంపస్లో అత్యంత లోతైన మార్పులు గమనించబడ్డాయి, గ్లుటాతియోన్ పెరాక్సిడేస్ మరియు మొత్తం పెరుగుదల. యాంటీఆక్సిడెంట్ సామర్థ్యాలు.
కీటోజెనిక్ డైట్, కీటోన్ ఈస్టర్లు (కీటోజెనిక్ డైట్ మరియు ఎక్సోజనస్ కీటోన్ బాడీస్ యొక్క చికిత్సా ఉపయోగం కూడా చూడండి), లేదా ?OHB అడ్మినిస్ట్రేషన్ ఇస్కీమిక్ స్ట్రోక్ మోడల్లలో న్యూరోప్రొటెక్షన్ను చూపుతుంది (రెహ్మాన్ మరియు ఇతరులు., 2014); పార్కిన్సన్స్ వ్యాధి (టైయు మరియు ఇతరులు, 2003); కేంద్ర నాడీ వ్యవస్థ ఆక్సిజన్ విషపూరిత నిర్భందించటం (D'Agostino et al., 2013); ఎపిలెప్టిక్ స్పామ్స్ (యం మరియు ఇతరులు, 2015); మైటోకాన్డ్రియాల్ ఎన్సెఫలోమయోపతి, లాక్టిక్ అసిడోసిస్ మరియు స్ట్రోక్-లాంటి (MELAS) ఎపిసోడ్స్ సిండ్రోమ్ (ఫ్రే మరియు ఇతరులు, 2016) మరియు అల్జీమర్స్ వ్యాధి (కున్నాన్ మరియు క్రాఫోర్డ్, 2003; యిన్ మరియు ఇతరులు., 2016). దీనికి విరుద్ధంగా, మైటోకాన్డ్రియల్ బయోజెనిసిస్ మరియు యాంటీఆక్సిడెంట్ సంతకాలు (లౌరిట్జెన్ మరియు ఇతరులు, 2016) పెరిగినప్పటికీ, అసాధారణ మైటోకాన్డ్రియల్ DNA మరమ్మత్తు యొక్క ట్రాన్స్జెనిక్ మౌస్ మోడల్లో కీటోజెనిక్ డైట్ ద్వారా న్యూరోడెజెనరేటివ్ పురోగతికి సంబంధించిన హిస్టోపాథలాజికల్ సాక్ష్యాలను ఇటీవలి నివేదిక ప్రదర్శించింది. ఇతర విరుద్ధమైన నివేదికలు అధిక కీటోన్ శరీర సాంద్రతలకు గురికావడం ఆక్సీకరణ ఒత్తిడిని కలిగిస్తుందని సూచిస్తున్నాయి. అధిక ?OHB లేదా AcAc మోతాదులు నైట్రిక్ ఆక్సైడ్ స్రావం, లిపిడ్ పెరాక్సిడేషన్, SOD యొక్క తగ్గిన వ్యక్తీకరణ, దూడ హెపటోసైట్లలో గ్లూటాతియోన్ పెరాక్సిడేస్ మరియు ఉత్ప్రేరకాలను ప్రేరేపించాయి, అయితే ఎలుక హెపటోసైట్లలో MAPK పాత్వే ఇండక్షన్ AcAcకి ఆపాదించబడింది కానీ ?OHB2004, 2014 ; షి మరియు ఇతరులు, 2016; షి మరియు ఇతరులు., XNUMX).
కలిసి తీసుకుంటే, చాలా నివేదికలు ?OHBని ఆక్సీకరణ ఒత్తిడిని అటెన్యుయేషన్కు అనుసంధానిస్తాయి, దాని పరిపాలన ROS/సూపెరాక్సైడ్ ఉత్పత్తిని నిరోధిస్తుంది, లిపిడ్ పెరాక్సిడేషన్ మరియు ప్రోటీన్ ఆక్సీకరణను నిరోధిస్తుంది, యాంటీఆక్సిడెంట్ ప్రోటీన్ స్థాయిలను పెంచుతుంది మరియు మైటోకాన్డ్రియల్ శ్వాసక్రియ మరియు ATP ఉత్పత్తిని మెరుగుపరుస్తుంది (Abdelmegeed et al., 2004; హేసెస్ ఎట్ అల్., 2008; జైన్ ఎట్ అల్., 1998; జైన్ ఎట్ అల్., 2002; కనికర్ల-మేరీ మరియు జైన్, 2015; మలూఫ్ మరియు ఇతరులు., 2007; మలౌఫ్ మరియు రో, 2008; మరోసి 2016al., టి 2003 et మరియు ఇతరులు, 2016; యిన్ మరియు ఇతరులు., 2003; జిగ్లెర్ మరియు ఇతరులు., 2002). AcAc ఆక్సిడేటివ్ స్ట్రెస్ యొక్క ఇండక్షన్తో ?OHB కంటే నేరుగా పరస్పర సంబంధం కలిగి ఉన్నప్పటికీ, ఈ ప్రభావాలు ఎల్లప్పుడూ భావి శోథ నిరోధక ప్రతిస్పందనల నుండి సులభంగా విడదీయబడవు (జైన్ మరియు ఇతరులు, 2015; కనికర్ల-మేరీ మరియు జైన్, 2016; కనికర్ల-మేరీ మరియు జైన్, 2016). అంతేకాకుండా, ప్లీయోట్రోపిక్ కీటోజెనిక్ డైట్ల ద్వారా అందించబడే స్పష్టమైన యాంటీఆక్సిడేటివ్ ప్రయోజనం కీటోన్ బాడీల ద్వారా ప్రసారం చేయబడకపోవచ్చు మరియు కీటోన్ బాడీల ద్వారా అందించబడిన న్యూరోప్రొటెక్షన్ పూర్తిగా ఆక్సీకరణ ఒత్తిడికి ఆపాదించబడదని పరిగణనలోకి తీసుకోవడం చాలా క్లిష్టమైనది. ఉదాహరణకు, గ్లూకోజ్ లేమి సమయంలో, కార్టికల్ న్యూరాన్లలో గ్లూకోజ్ లేమి యొక్క నమూనాలో, ?OHB ఆటోఫాగిక్ ఫ్లక్స్ను ప్రేరేపించింది మరియు ఆటోఫాగోజోమ్ చేరడం నిరోధించింది, ఇది న్యూరోనల్ డెత్ తగ్గడంతో సంబంధం కలిగి ఉంటుంది (కాంబెరోస్-లూనా మరియు ఇతరులు., 3). d-?OHB HDAC నిరోధం ద్వారా కానానికల్ యాంటీఆక్సిడెంట్ ప్రోటీన్లు FOXO2016a, SOD, MnSOD మరియు ఉత్ప్రేరకాలను కూడా ప్రేరేపిస్తుంది (నాగావో మరియు ఇతరులు, 2013; షిమాజు మరియు ఇతరులు., XNUMX).
నాన్-ఆల్కహాలిక్ ఫ్యాటీ లివర్ డిసీజ్ (NAFLD) మరియు కీటోన్ బాడీ మెటబాలిజం
పాశ్చాత్య దేశాలలో కాలేయ వ్యాధికి ఊబకాయం-సంబంధిత NAFLD మరియు నాన్-ఆల్కహాలిక్ స్టీటోహెపటైటిస్ (NASH) అత్యంత సాధారణ కారణాలు (Rinella మరియు Sanyal, 2016), మరియు NASH- ప్రేరిత కాలేయ వైఫల్యం కాలేయ మార్పిడికి అత్యంత సాధారణ కారణాలలో ఒకటి. హెపటోసైట్స్> 5% కాలేయ బరువు (NAFL)లో ట్రయాసిల్గ్లిసరాల్స్ను అధికంగా నిల్వ చేయడం వల్ల కాలేయ పనితీరు క్షీణించదు, మానవులలో NAFLDకి పురోగతి దైహిక ఇన్సులిన్ నిరోధకత మరియు టైప్ 2 మధుమేహం వచ్చే ప్రమాదంతో పరస్పర సంబంధం కలిగి ఉంటుంది మరియు వ్యాధికారక ఉత్పత్తికి దోహదం చేస్తుంది. హృదయ సంబంధ వ్యాధులు మరియు దీర్ఘకాలిక మూత్రపిండ వ్యాధి (ఫాబ్బ్రిని మరియు ఇతరులు, 2009; టార్గర్ మరియు ఇతరులు, 2010; టార్గర్ మరియు బైర్నే, 2013). NAFLD మరియు NASH యొక్క వ్యాధికారక విధానాలు అసంపూర్తిగా అర్థం చేసుకోబడ్డాయి, అయితే హెపాటోసైట్ జీవక్రియ యొక్క అసాధారణతలు, హెపాటోసైట్ ఆటోఫాగి మరియు ఎండోప్లాస్మిక్ రెటిక్యులం ఒత్తిడి, హెపాటిక్ రోగనిరోధక కణాల పనితీరు, కొవ్వు కణజాల వాపు మరియు దైహిక తాపజనక మధ్యవర్తులు (Fabbrini et al., Chalasanisuka 2009; ; టార్గర్ మరియు ఇతరులు., 2013; యాంగ్ మరియు ఇతరులు., 2010). కార్బోహైడ్రేట్, లిపిడ్ మరియు అమైనో యాసిడ్ జీవక్రియ యొక్క కదలికలు మానవులలో మరియు నమూనా జీవులలో ఊబకాయం, మధుమేహం మరియు NAFLDకి దోహదం చేస్తాయి [సమీక్షించబడింది (Farese et al., 2010; Lin and Accili, 2012; Newgard, 2011; Samuel మరియు షుల్మాన్, 2012; సన్ అండ్ లాజర్, 2012)]. సైటోప్లాస్మిక్ లిపిడ్ జీవక్రియలో హెపాటోసైట్ అసాధారణతలు సాధారణంగా NAFLD (Fabbrini et al., 2013b)లో గమనించవచ్చు, కొవ్వుల ఆక్సీకరణ పారవేయడాన్ని నియంత్రించే మైటోకాన్డ్రియల్ జీవక్రియ యొక్క పాత్ర NAFLD వ్యాధికారక ఉత్పత్తిలో తక్కువ స్పష్టంగా ఉంటుంది. మైటోకాన్డ్రియల్ జీవక్రియ యొక్క అసాధారణతలు NAFLD/NASH పాథోజెనిసిస్లో సంభవిస్తాయి మరియు దోహదం చేస్తాయి (హయోటిలైన్ మరియు ఇతరులు, 2010; సర్విడియో మరియు ఇతరులు., 2016; సర్విడియో మరియు ఇతరులు., 2011; వీ మరియు ఇతరులు., 2008). సాధారణం ఉంది (ఫెలిగ్ మరియు ఇతరులు, 2008; ఐయోజో మరియు ఇతరులు., 1974; కొలియాకి మరియు ఇతరులు., 2010; సతపతి మరియు ఇతరులు., 2015; సతపతి మరియు ఇతరులు., 2015; సన్నీ మరియు ఇతరులు., 2012) కానీ ఏకరూపం కాదు కొలియాకి మరియు రోడెన్, 2011; పెర్రీ మరియు ఇతరులు., 2013; రెక్టార్ మరియు ఇతరులు., 2016) ఏకాభిప్రాయం, మంచి NASH అభివృద్ధికి ముందు, హెపాటిక్ మైటోకాన్డ్రియల్ ఆక్సీకరణ మరియు ముఖ్యంగా కొవ్వు ఆక్సీకరణ, స్థూలకాయంలో వ్యవస్థాగతంగా వృద్ధి చెందుతుంది. , మరియు NAFLD. NAFLD పురోగమిస్తున్న కొద్దీ, వ్యక్తిగత మైటోకాండ్రియాలో కూడా ఆక్సీకరణ సామర్థ్యం హెటెరోజెనిటీ ఉద్భవిస్తుంది మరియు చివరికి ఆక్సీకరణ పనితీరు బలహీనపడుతుంది (కోలియాకి మరియు ఇతరులు, 2010; రెక్టర్ మరియు ఇతరులు., 2015; సతపతి మరియు ఇతరులు., 2010etal; ., 2008).
కీటోజెనిసిస్ తరచుగా హెపాటిక్ కొవ్వు ఆక్సీకరణకు ప్రాక్సీగా ఉపయోగించబడుతుంది. జంతు నమూనాలలో మరియు మానవులలో NAFLD పురోగమిస్తున్నందున కీటోజెనిసిస్ యొక్క లోపాలు ఉద్భవించాయి. అసంపూర్తిగా నిర్వచించబడిన మెకానిజమ్స్ ద్వారా, హైపర్ఇన్సులినిమియా కీటోజెనిసిస్ను అణిచివేస్తుంది, లీన్ కంట్రోల్లతో పోలిస్తే హైపోకెటోనిమియాకు దోహదపడవచ్చు (బెర్గ్మాన్ మరియు ఇతరులు, 2007; బికెర్టన్ మరియు ఇతరులు., 2008; సతాపతి మరియు ఇతరులు., 2012 etal., 2009 etal., 2011 , 2005; వైస్ మరియు ఇతరులు, 2015). ఏది ఏమైనప్పటికీ, NAFLDని అంచనా వేయడానికి కీటోన్ శరీర సాంద్రతలను ప్రసరించే సామర్థ్యం వివాదాస్పదంగా ఉంది (M'nnisté et al., 2001; Sanyal et al., 2012). జంతు నమూనాలలో బలమైన పరిమాణాత్మక మాగ్నెటిక్ రెసొనెన్స్ స్పెక్ట్రోస్కోపిక్ పద్ధతులు మితమైన ఇన్సులిన్ నిరోధకతతో పెరిగిన కీటోన్ టర్నోవర్ రేటును వెల్లడించాయి, అయితే మరింత తీవ్రమైన ఇన్సులిన్ నిరోధకతతో తగ్గిన రేట్లు స్పష్టంగా కనిపించాయి (సతపతి మరియు ఇతరులు, 2010; సన్నీ మరియు ఇతరులు., 2008). కొవ్వు కాలేయం ఉన్న స్థూలకాయ మానవులలో, కీటోజెనిక్ రేటు సాధారణం (బికర్టన్ మరియు ఇతరులు, 2011; సన్నీ మరియు ఇతరులు., 4), అందువల్ల, హెపాటోసైట్లలో పెరిగిన కొవ్వు ఆమ్ల లోడ్కు సంబంధించి కీటోజెనిసిస్ రేట్లు తగ్గుతాయి. పర్యవసానంగా, ?-ఆక్సీకరణ-ఉత్పన్నమైన ఎసిటైల్-CoA TCA చక్రంలో టెర్మినల్ ఆక్సీకరణకు మళ్ళించబడవచ్చు, టెర్మినల్ ఆక్సీకరణను పెంచుతుంది, అనాప్లెరోసిస్/కాటాప్లెరోసిస్ ద్వారా ఫాస్ఫోఎనోల్పైరువేట్-నడిచే గ్లూకోనోజెనిసిస్ మరియు ఆక్సీకరణ ఒత్తిడి. ఎసిటైల్-CoA మైటోకాండ్రియా నుండి సిట్రేట్గా ఎగుమతి చేయబడవచ్చు, ఇది లిపోజెనిసిస్కు పూర్వగామి సబ్స్ట్రేట్ (Fig. 2015) (Satapati et al., 2012; Satapati et al., 2015; Solinas et al., 2012). కీటోజెనిసిస్ ఇన్సులిన్కు తక్కువ ప్రతిస్పందిస్తుంది లేదా దీర్ఘకాలిక ఊబకాయంతో ఉపవాసం (సతపతి మరియు ఇతరులు, 1), దీని యొక్క అంతర్లీన విధానాలు మరియు దిగువ పరిణామాలు అసంపూర్ణంగా అర్థం చేసుకోబడ్డాయి. mTORC2016 ఇన్సులిన్ సిగ్నలింగ్ (కుసెజోవా మరియు ఇతరులు, 1) దిగువన ఉండే పద్ధతిలో కీటోజెనిసిస్ను అణిచివేస్తుందని ఇటీవలి ఆధారాలు సూచిస్తున్నాయి, ఇది mTORC2 PPAR?-మధ్యవర్తిత్వ Hmgcs2010 ఇండక్షన్ (Sengupta et al., 2) నిరోధిస్తుందని పరిశీలనలకు అనుగుణంగా ఉంటుంది. HMGCS1 మరియు SCOT/OXCTXNUMX యొక్క నియంత్రణ కూడా చూడండి).

మా బృందం నుండి ప్రాథమిక పరిశీలనలు కీటోజెనిక్ లోపం యొక్క ప్రతికూల హెపాటిక్ పరిణామాలను సూచిస్తున్నాయి (కోటర్ మరియు ఇతరులు., 2014). బలహీనమైన కెటోజెనిసిస్, కార్బోహైడ్రేట్-రిప్లీట్ మరియు తద్వారా నాన్-కీటోజెనిక్ స్టేట్స్లో కూడా అసాధారణమైన గ్లూకోజ్ జీవక్రియకు దోహదం చేస్తుంది మరియు స్టీటోహెపటైటిస్ను రేకెత్తిస్తుంది అనే పరికల్పనను పరీక్షించడానికి, మేము యాంటీసెన్స్ లక్ష్యమైన ఒలిగోన్యూక్లియోటైడ్ల నిర్వహణ ద్వారా గుర్తించబడిన కీటోజెనిక్ లోపం యొక్క మౌస్ నమూనాను రూపొందించాము. Hmgcs2. ప్రామాణిక తక్కువ-కొవ్వు చౌ-తినిపించిన వయోజన ఎలుకలలో HMGCS2 కోల్పోవడం తేలికపాటి హైపర్గ్లైసీమియాకు కారణమైంది మరియు వందలాది హెపాటిక్ మెటాబోలైట్ల ఉత్పత్తిని గణనీయంగా పెంచింది, వీటిలో సూట్ లిపోజెనిసిస్ యాక్టివేషన్ను గట్టిగా సూచించింది. తగినంత కీటోజెనిసిస్తో ఎలుకలకు అధిక కొవ్వు ఆహారం ఇవ్వడం వల్ల విస్తృతమైన హెపాటోసైట్ గాయం మరియు వాపు ఏర్పడింది. ఈ పరిశోధనలు (i) కీటోజెనిసిస్ అనేది నిష్క్రియ ఓవర్ఫ్లో పాత్వే కాదు, హెపాటిక్ మరియు ఇంటిగ్రేటెడ్ ఫిజియోలాజికల్ హోమియోస్టాసిస్లో డైనమిక్ నోడ్, మరియు (ii) NAFLD/NASHని తగ్గించడానికి వివేకవంతమైన కీటోజెనిక్ ఆగ్మెంటేషన్ మరియు హెపాటిక్ గ్లూకోజ్ జీవక్రియ యొక్క క్రమరహితమైన జీవక్రియ విలువైనది అనే కేంద్ర పరికల్పనలకు మద్దతు ఇస్తుంది. .
బలహీనమైన కీటోజెనిసిస్ హెపాటిక్ గాయం మరియు మార్చబడిన గ్లూకోజ్ హోమియోస్టాసిస్కు ఎలా దోహదపడుతుంది? మొదటి పరిశీలన ఏమిటంటే, అపరాధి కీటోజెనిక్ ఫ్లక్స్ యొక్క లోపమా, లేదా కీటోన్ల లోపమా. n-3 బహుళఅసంతృప్త కొవ్వు ఆమ్లాలకు ప్రతిస్పందనగా కీటోన్ శరీరాలు ఆక్సీకరణ ఒత్తిడి-ప్రేరిత హెపాటిక్ గాయాన్ని తగ్గించవచ్చని ఇటీవలి నివేదిక సూచిస్తుంది (పావ్లాక్ మరియు ఇతరులు., 2015). హెపటోసైట్లలో SCOT వ్యక్తీకరణ లేకపోవడం వల్ల, కీటోన్ శరీరాలు ఆక్సీకరణం చెందవు, కానీ అవి లైపోజెనిసిస్కు దోహదపడతాయి మరియు వాటి ఆక్సీకరణతో సంబంధం లేకుండా అనేక రకాల సిగ్నలింగ్ పాత్రలను అందిస్తాయి (కీటోన్ బాడీల యొక్క నాన్-ఆక్సిడేటివ్ మెటబాలిక్ ఫేట్స్ మరియు ?OHBని కూడా చూడండి. ఒక సిగ్నలింగ్ మధ్యవర్తి). హెపాటోసైట్-ఉత్పన్నమైన కీటోన్ బాడీలు హెపాటిక్ అసినస్లోని పొరుగు కణ రకాలకు సిగ్నల్ మరియు/లేదా మెటాబోలైట్గా ఉపయోగపడే అవకాశం ఉంది, ఇందులో స్టెలేట్ కణాలు మరియు కుఫ్ఫర్ సెల్ మాక్రోఫేజ్లు ఉన్నాయి. మాక్రోఫేజ్లు కీటోన్ బాడీలను ఆక్సీకరణం చేయలేవని అందుబాటులో ఉన్న పరిమిత సాహిత్యం సూచిస్తున్నప్పటికీ, ఇది క్లాసికల్ మెథడాలజీలను ఉపయోగించి మాత్రమే కొలుస్తారు మరియు పెరిటోనియల్ మాక్రోఫేజ్లలో మాత్రమే కొలుస్తారు (Newsholme et al., 1986; Newsholme et al., 1987), ఇది తిరిగి- అని సూచిస్తుంది. ఎముక మజ్జ-ఉత్పన్నమైన మాక్రోఫేజ్లలో సమృద్ధిగా ఉన్న SCOT వ్యక్తీకరణను అంచనా వేయడం సముచితం (యుమ్ మరియు ఇతరులు, 2015).
హెపాటోసైట్ కీటోజెనిక్ ఫ్లక్స్ సైటోప్రొటెక్టివ్ కూడా కావచ్చు. రక్షిత యంత్రాంగాలు కీటోజెనిసిస్పై ఆధారపడి ఉండకపోవచ్చు, తక్కువ కార్బోహైడ్రేట్ కీటోజెనిక్ ఆహారాలు NAFLD యొక్క మెరుగుదలతో సంబంధం కలిగి ఉన్నాయి (బ్రౌనింగ్ మరియు ఇతరులు, 2011; ఫోస్టర్ మరియు ఇతరులు., 2010; కనీ మరియు ఇతరులు., 2014; షుగర్ మరియు క్రాఫోర్డ్) . మా పరిశీలనలు హెపాటోసైట్ కీటోజెనిసిస్ TCA సైకిల్ ఫ్లక్స్, అనాప్లెరోటిక్ ఫ్లక్స్, ఫాస్ఫోఎనోల్పైరువేట్-డెరైవ్డ్ గ్లూకోనోజెనిసిస్ (కోటర్ మరియు ఇతరులు, 2012) మరియు గ్లైకోజెన్ టర్నోవర్ను ఫీడ్బ్యాక్ చేసి నియంత్రించవచ్చని సూచిస్తున్నాయి. కీటోజెనిక్ బలహీనత TCA ఫ్లక్స్ను పెంచడానికి ఎసిటైల్-CoAని నిర్దేశిస్తుంది, కాలేయంలో పెరిగిన ROS-మధ్యవర్తిత్వ గాయంతో ముడిపడి ఉంది (సతపతి మరియు ఇతరులు, 2014; సతపతి మరియు ఇతరులు., 2015); సైటోటాక్సిక్ను నిరూపించగల డి నోవో సింథసైజ్డ్ లిపిడ్ జాతులలోకి కార్బన్ను మళ్లించడాన్ని బలవంతం చేస్తుంది; మరియు NAD+కి NADH రీ-ఆక్సీకరణను నిరోధిస్తుంది (కోటర్ మరియు ఇతరులు, 2012) (Fig. 2014). కలిసి తీసుకుంటే, సాపేక్ష కీటోజెనిక్ లోపం దుర్వినియోగం కావచ్చు, హైపర్గ్లైసీమియాకు దోహదం చేస్తుంది, స్టీటోహెపటైటిస్ను రేకెత్తిస్తుంది మరియు ఈ యంత్రాంగాలు మానవుల NAFLD/NASHలో పనిచేస్తాయా లేదా అనే విధానాలను పరిష్కరించడానికి భవిష్యత్తులో ప్రయోగాలు అవసరం. ఎపిడెమియోలాజికల్ సాక్ష్యం ప్రకారం స్టీటోహెపటైటిస్ యొక్క పురోగతి సమయంలో బలహీనమైన కీటోజెనిసిస్ (ఎంబేడ్ మరియు ఇతరులు, 4; మారినౌ మరియు ఇతరులు., 2016; మన్నిస్టే మరియు ఇతరులు., 2011; ప్రామ్ఫాల్క్ మరియు ఇతరులు., 2015; సఫాయీ 2015; 2016 ఆల్.) హెపాటిక్ కీటోజెనిసిస్ను పెంచే చికిత్సలు ప్రయోజనకరమైనవిగా నిరూపించగలవు (డెగిరోలామో మరియు ఇతరులు, 2016; హోండా మరియు ఇతరులు., 2016).
కీటోన్ శరీరాలు మరియు గుండె వైఫల్యం (HF)
జీవక్రియ రేటు 400 kcal/kg/రోజుకు మించి, మరియు 6–35 kg ATP/రోజు టర్నోవర్తో, గుండె అత్యధిక శక్తి వ్యయం మరియు ఆక్సీకరణ డిమాండ్ కలిగిన అవయవం (అష్రాఫియన్ మరియు ఇతరులు, 2007; వాంగ్ మరియు ఇతరులు., 2010b). మయోకార్డియల్ ఎనర్జీ టర్నోవర్లో ఎక్కువ భాగం మైటోకాండ్రియాలో నివసిస్తుంది మరియు ఈ సరఫరాలో 70% FAO నుండి ఉద్భవించింది. సాధారణ పరిస్థితులలో గుండె సర్వభక్షకమైనది మరియు అనువైనది, కానీ వ్యాధికారక రీమోడలింగ్ గుండె (ఉదా, రక్తపోటు లేదా మయోకార్డియల్ ఇన్ఫార్క్షన్ కారణంగా) మరియు డయాబెటిక్ గుండె ప్రతి ఒక్కటి జీవక్రియకు అనువుగా మారతాయి (బలాస్సే మరియు ఫెరీ, 1989; BING, 1954; ఫుకావో మరియు ఇతరులు., 2004. ; Lopaschuk et al., 2010; Taegtmeyer et al., 1980; Taegtmeyer et al., 2002; యంగ్ మరియు ఇతరులు., 2002). నిజానికి, మౌస్ మోడల్లలో కార్డియాక్ ఫ్యూయల్ మెటబాలిజం యొక్క జన్యుపరంగా ప్రోగ్రామ్ చేయబడిన అసాధారణతలు కార్డియోమయోపతిని రేకెత్తిస్తాయి (కార్లే మరియు ఇతరులు, 2014; న్యూబౌర్, 2007). శారీరక పరిస్థితులలో సాధారణ హృదయాలు కొవ్వు ఆమ్లం మరియు గ్లూకోజ్ ఆక్సీకరణ ఖర్చుతో వాటి డెలివరీకి అనులోమానుపాతంలో కీటోన్ శరీరాలను ఆక్సీకరణం చేస్తాయి మరియు మయోకార్డియం యూనిట్ ద్రవ్యరాశికి అత్యధిక కీటోన్ శరీర వినియోగదారుగా ఉంది (BING, 1954; క్రాఫోర్డ్ మరియు ఇతరులు., 2009; గార్లాండ్ మరియు ఇతరులు. ., 1962; హాసెల్బైంక్ మరియు ఇతరులు., 2003; జెఫ్రీ మరియు ఇతరులు., 1995; పెల్లెటియర్ మరియు ఇతరులు., 2007; టార్డిఫ్ మరియు ఇతరులు., 2001; యాన్ మరియు ఇతరులు., 2009). ఫ్యాటీ యాసిడ్ ఆక్సీకరణతో పోలిస్తే, కీటోన్ బాడీలు మరింత శక్తివంతంగా సమర్థవంతంగా పనిచేస్తాయి, పెట్టుబడి పెట్టిన ఆక్సిజన్ అణువుకు (P/O నిష్పత్తి) ATP సంశ్లేషణ కోసం ఎక్కువ శక్తిని అందజేస్తుంది (కాశీవాయ మరియు ఇతరులు, 2010; సాటో మరియు ఇతరులు., 1995; వీచ్, 2004) . కీటోన్ బాడీ ఆక్సీకరణ కూడా FAO కంటే అధిక శక్తిని ఇస్తుంది, ubiquinone ఆక్సీకరణం చెందుతుంది, ఇది ఎలక్ట్రాన్ రవాణా గొలుసులో రెడాక్స్ స్పాన్ను పెంచుతుంది మరియు ATPని సంశ్లేషణ చేయడానికి మరింత శక్తిని అందుబాటులో ఉంచుతుంది (సాటో మరియు ఇతరులు, 1995; వీచ్, 2004). కీటోన్ శరీరాల ఆక్సీకరణ ROS ఉత్పత్తిని కూడా తగ్గించవచ్చు, తద్వారా ఆక్సీకరణ ఒత్తిడి (వీచ్, 2004).
ప్రాథమిక ఇంటర్వెన్షనల్ మరియు అబ్జర్వేషనల్ స్టడీస్ గుండెలో కీటోన్ బాడీల సంభావ్య రక్షిత పాత్రను సూచిస్తున్నాయి. ప్రయోగాత్మక ఇస్కీమియా/రిపెర్ఫ్యూజన్ గాయం సందర్భంలో, కీటోన్ శరీరాలు సంభావ్య కార్డియోప్రొటెక్టివ్ ప్రభావాలను అందించాయి (అల్-జైద్ మరియు ఇతరులు, 2007; వాంగ్ మరియు ఇతరులు., 2008), బహుశా గుండెలో మైటోకాన్డ్రియల్ సమృద్ధి పెరగడం లేదా కీలకమైన ఫాస్ఫోరీ ఆక్సిడేటివ్ ఆక్సీకరణ యొక్క అప్-రెగ్యులేషన్ కారణంగా కావచ్చు. మధ్యవర్తులు (స్నోరెక్ మరియు ఇతరులు, 2012; జూ మరియు ఇతరులు., 2002). ఇటీవలి అధ్యయనాలు ఎలుకల (అబెర్ట్ మరియు ఇతరులు, 2016) మరియు మానవుల (బేడీ మరియు ఇతరులు, 2016) విఫలమైన హృదయాలలో కీటోన్ శరీర వినియోగం పెరిగిందని సూచిస్తున్నాయి, మానవులలో ముందస్తు పరిశీలనలకు మద్దతు ఇస్తోంది (BING, 1954; Fukao et al., 2000; జనార్ధన్ మరియు ఇతరులు., 2011; లాంగో మరియు ఇతరులు., 2004; రుడాల్ఫ్ మరియు షింజ్, 1973; టిల్డన్ మరియు కార్న్బ్లాత్, 1972). గుండె ఆగిపోయిన రోగులలో సర్క్యులేటింగ్ కీటోన్ బాడీ సాంద్రతలు పెరుగుతాయి, ఒత్తిడిని పూరించడానికి ప్రత్యక్ష నిష్పత్తిలో, పరిశీలనల విధానం మరియు ప్రాముఖ్యత తెలియదు (కుపారి మరియు ఇతరులు, 1995; లోమ్మీ మరియు ఇతరులు., 1996; లోమ్మీ మరియు ఇతరులు., 1997; నీలీ మరియు ఇతరులు ., 1972), అయితే కార్డియోమయోసైట్స్లో సెలెక్టివ్ SCOT లోపం ఉన్న ఎలుకలు శస్త్రచికిత్స ద్వారా ప్రేరేపిత ఒత్తిడి ఓవర్లోడ్ గాయానికి ప్రతిస్పందనగా వేగవంతమైన పాథలాజికల్ వెంట్రిక్యులర్ రీమోడలింగ్ మరియు ROS సంతకాలను ప్రదర్శిస్తాయి (Schugar et al., 2014).
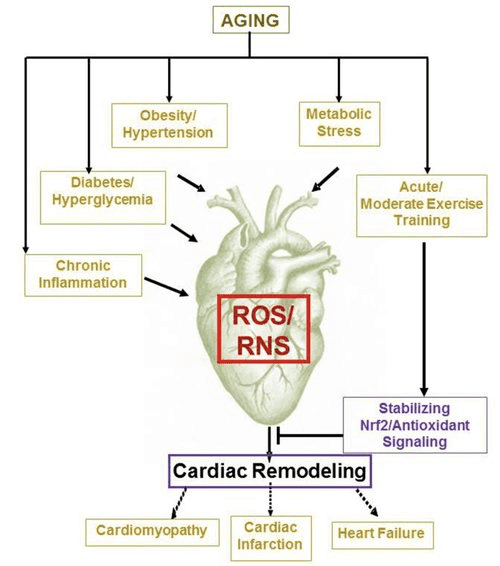
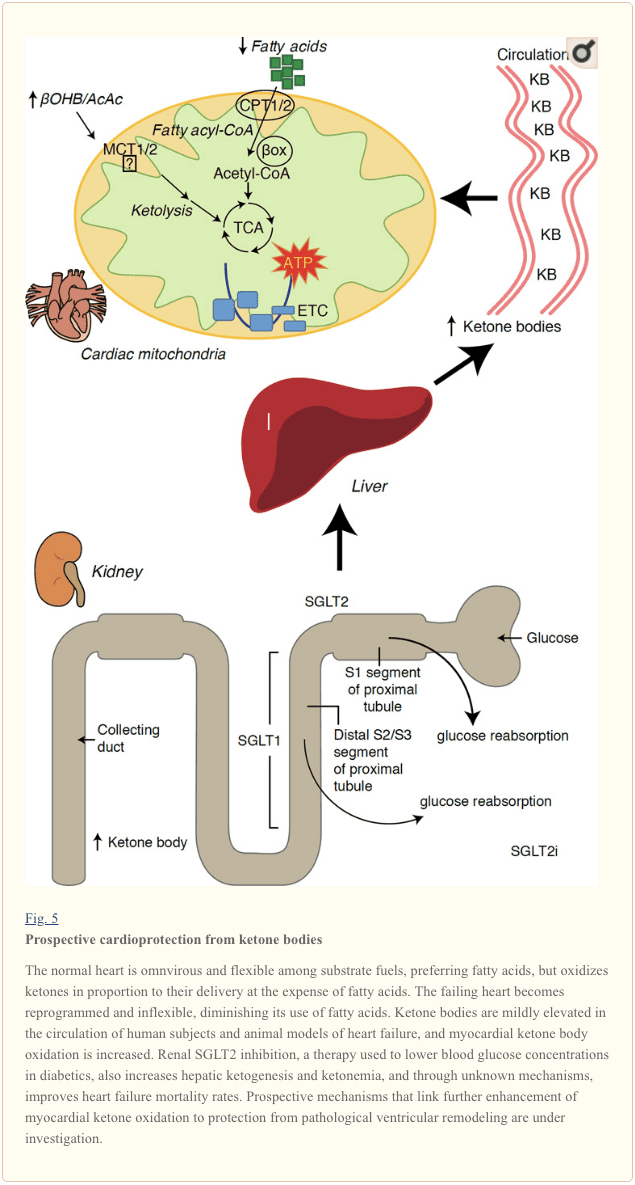
మధుమేహ చికిత్సలో ఇటీవలి చమత్కార పరిశీలనలు మయోకార్డియల్ కీటోన్ జీవక్రియ మరియు పాథలాజికల్ వెంట్రిక్యులర్ రీమోడలింగ్ (Fig. 5) మధ్య సంభావ్య సంబంధాన్ని వెల్లడించాయి. మూత్రపిండ ప్రాక్సిమల్ ట్యూబ్యులర్ సోడియం/గ్లూకోజ్ కో-ట్రాన్స్పోర్టర్ 2 (SGLT2i) యొక్క నిరోధం మానవులలో కీటోన్ శరీర సాంద్రతలను ప్రసరింపజేయడాన్ని పెంచుతుంది (ఫెర్రానిని మరియు ఇతరులు, 2016a; ఇనాగాకి మరియు ఇతరులు., 2015) మరియు ఎలుకలు (సుజుకి 2014., ద్వారా) పెరిగింది హెపాటిక్ కీటోజెనిసిస్ (ఫెరానిని మరియు ఇతరులు, 2014; ఫెర్రానిని మరియు ఇతరులు, 2016a; కాట్జ్ మరియు లీటర్, 2015; ముదలియార్ మరియు ఇతరులు., 2015). ఆశ్చర్యకరంగా, ఈ ఏజెంట్లలో కనీసం ఒకరు HF ఆసుపత్రిలో చేరడాన్ని తగ్గించారు (ఉదా, EMPA-REG అవుట్కమ్ ట్రయల్ ద్వారా వెల్లడైంది), మరియు మెరుగైన హృదయనాళ మరణాలు (ఫిట్చెట్ మరియు ఇతరులు, 2016; సోనెస్సన్ మరియు ఇతరులు., 2016; వు మరియు ఇతరులు., 2016a ; జిన్మాన్ మరియు ఇతరులు., 2015). లింక్ చేయబడిన SGLT2iకి లాభదాయకమైన HF ఫలితాల వెనుక ఉన్న డ్రైవర్ మెకానిజమ్స్ చురుకుగా చర్చనీయాంశంగా ఉన్నప్పటికీ, మనుగడ ప్రయోజనం మల్టిఫ్యాక్టోరియల్గా ఉంటుంది, బహుశా కీటోసిస్తో సహా, బరువు, రక్తపోటు, గ్లూకోజ్ మరియు యూరిక్ యాసిడ్ స్థాయిలు, ధమనుల దృఢత్వం, సానుభూతి నాడీ వ్యవస్థ, ద్రవాభిసరణ వంటి వాటిపై ప్రయోజనకరమైన ప్రభావాలు కూడా ఉన్నాయి. డైయూరిసిస్/తగ్గిన ప్లాస్మా వాల్యూమ్, మరియు హెమటోక్రిట్ పెరిగింది (రాజ్ మరియు కాహ్న్, 2016; వల్లన్ మరియు థామ్సన్, 2016). కలిసి చూస్తే, హెచ్ఎఫ్ రోగులలో లేదా హెచ్ఎఫ్ అభివృద్ధి చెందే ప్రమాదం ఎక్కువగా ఉన్నవారిలో చికిత్సాపరంగా కీటోనెమియా పెరుగుతుందనే భావన వివాదాస్పదంగానే ఉంది, అయితే ప్రీ-క్లినికల్ మరియు క్లినికల్ స్టడీస్లో చురుకైన పరిశోధనలో ఉంది (ఫెర్రానిని మరియు ఇతరులు, 2016బి; కోల్విజ్ మరియు ఇతరులు., 2016; లోపాస్చుక్ మరియు వర్మ, 2016; ముదలియార్ మరియు ఇతరులు., 2016; టైగ్ట్మేయర్, 2016).
క్యాన్సర్ జీవశాస్త్రంలో కీటోన్ బాడీస్
కీటోన్ బాడీలు మరియు క్యాన్సర్ మధ్య సంబంధాలు వేగంగా అభివృద్ధి చెందుతున్నాయి, అయితే జంతు నమూనాలు మరియు మానవులు రెండింటిలో చేసిన అధ్యయనాలు విభిన్న ముగింపులను అందించాయి. కీటోన్ జీవక్రియ డైనమిక్ మరియు పోషక స్థితికి ప్రతిస్పందిస్తుంది కాబట్టి, ఖచ్చితమైన-గైడెడ్ పోషకాహార చికిత్సల సంభావ్యత కారణంగా క్యాన్సర్కు జీవసంబంధమైన కనెక్షన్లను కొనసాగించడం మనోహరంగా ఉంటుంది. వేగవంతమైన కణాల విస్తరణ మరియు పెరుగుదలను నిర్వహించడానికి క్యాన్సర్ కణాలు జీవక్రియ రీప్రోగ్రామింగ్కు లోనవుతాయి (డెనికోలా మరియు కాంట్లీ, 2015; పావ్లోవా మరియు థాంప్సన్, 2016). క్యాన్సర్ కణ జీవక్రియలో క్లాసికల్ వార్బర్గ్ ప్రభావం శక్తిని బదిలీ చేయడానికి మరియు ఆక్సీకరణ ఫాస్ఫోరైలేషన్ మరియు పరిమిత మైటోకాన్డ్రియల్ శ్వాసక్రియపై తక్కువ ఆధారపడటాన్ని భర్తీ చేయడానికి గ్లైకోలిసిస్ మరియు లాక్టిక్ యాసిడ్ కిణ్వ ప్రక్రియ యొక్క ప్రధాన పాత్ర నుండి పుడుతుంది (డి ఫేటర్ మరియు ఇతరులు, 2016; గ్రాబాకా మరియు ఇతరులు., 2016; కాంగ్ మరియు ఇతరులు., 2015; పోఫ్ మరియు ఇతరులు., 2014; శుక్లా మరియు ఇతరులు., 2014). గ్లూకోజ్ కార్బన్ ప్రధానంగా గ్లైకోలిసిస్, పెంటోస్ ఫాస్ఫేట్ పాత్వే మరియు లిపోజెనిసిస్ ద్వారా నిర్దేశించబడుతుంది, ఇవి కణితి బయోమాస్ విస్తరణకు అవసరమైన మధ్యవర్తులను అందిస్తాయి (గ్రాబాకా మరియు ఇతరులు, 2016; శుక్లా మరియు ఇతరులు., 2014; యోషి మరియు ఇతరులు., 2015). అసిటేట్, గ్లుటామైన్ మరియు అస్పార్టేట్ (జావోర్స్కీ మరియు ఇతరులు, 2016; సుల్లివన్ మరియు ఇతరులు., 2015)తో సహా ప్రత్యామ్నాయ ఇంధన వనరులను ఉపయోగించుకునే సామర్థ్యం ద్వారా గ్లూకోజ్ లేమికి క్యాన్సర్ కణాలను స్వీకరించడం జరుగుతుంది. ఉదాహరణకు, పైరువేట్కు పరిమితం చేయబడిన యాక్సెస్ కార్బాక్సిలేషన్ ద్వారా గ్లుటామైన్ను ఎసిటైల్-CoAగా మార్చగల క్యాన్సర్ కణాల సామర్థ్యాన్ని వెల్లడిస్తుంది, ఇది శక్తివంతమైన మరియు అనాబాలిక్ అవసరాలను రెండింటినీ నిర్వహిస్తుంది (యాంగ్ మరియు ఇతరులు, 2014). అసిటేట్ను ఇంధనంగా ఉపయోగించడం అనేది క్యాన్సర్ కణాల యొక్క ఆసక్తికరమైన అనుసరణ (కామర్ఫోర్డ్ మరియు ఇతరులు, 2014; జావోర్స్కీ మరియు ఇతరులు., 2016; మషిమో మరియు ఇతరులు., 2014; రైట్ మరియు సిమోన్, 2016; యోషి మరియు ఇతరులు., 2015). అసిటేట్ కూడా లిపోజెనిసిస్కు ఒక ఉపరితలం, ఇది కణితి కణాల విస్తరణకు కీలకం, మరియు ఈ లిపోజెనిక్ వాహిక యొక్క లాభం తక్కువ రోగి మనుగడ మరియు ఎక్కువ కణితి భారంతో సంబంధం కలిగి ఉంటుంది (కామర్ఫోర్డ్ మరియు ఇతరులు, 2014; మాషిమో మరియు ఇతరులు., 2014; యోషి మరియు ఇతరులు. ., 2015).
క్యాన్సర్ లేని కణాలు గ్లూకోజ్ లేమి సమయంలో తమ శక్తి వనరులను గ్లూకోజ్ నుండి కీటోన్ బాడీలకు సులభంగా మారుస్తాయి. క్యాన్సర్ కణ రకాల్లో ఈ ప్లాస్టిసిటీ మరింత వేరియబుల్ కావచ్చు, కానీ వివోలో అమర్చిన మెదడు కణితులు [2,4-13C2]-?OHB చుట్టూ ఉన్న మెదడు కణజాలం (De Feyter et al., 2016) స్థాయికి ఆక్సీకరణం చెందాయి. రివర్స్ వార్బర్గ్ ఎఫెక్ట్ లేదా రెండు కంపార్ట్మెంట్ ట్యూమర్ మెటబాలిజం మోడల్లు క్యాన్సర్ కణాలు ప్రక్కనే ఉన్న ఫైబ్రోబ్లాస్ట్లలో ?OHB ఉత్పత్తిని ప్రేరేపిస్తాయని ఊహిస్తూ, కణితి కణాల శక్తి అవసరాలను అందిస్తాయి (బోన్యూసెల్లి మరియు ఇతరులు, 2010; మార్టినెజ్-ఔట్స్చూర్న్., 2012 et) . కాలేయంలో, హెపాటోసెల్యులర్ కార్సినోమా (హెపటోమా) కణాలలో కీటోజెనిసిస్ నుండి కీటోన్ ఆక్సీకరణకు హెపటోసైట్లలో మార్పు రెండు హెపటోమా సెల్ లైన్లలో గమనించిన BDH1 మరియు SCOT కార్యకలాపాల క్రియాశీలతకు అనుగుణంగా ఉంటుంది (జాంగ్ మరియు ఇతరులు, 1989). నిజానికి, హెపటోమా కణాలు OXCT1 మరియు BDH1ని వ్యక్తీకరిస్తాయి మరియు కీటోన్లను ఆక్సీకరణం చేస్తాయి, కానీ సీరం ఆకలితో ఉన్నప్పుడు మాత్రమే (హువాంగ్ మరియు ఇతరులు., 2016). ప్రత్యామ్నాయంగా, ట్యూమర్ సెల్ కీటోజెనిసిస్ కూడా ప్రతిపాదించబడింది. కీటోజెనిక్ జన్యు వ్యక్తీకరణలో డైనమిక్ మార్పులు పెద్దప్రేగు ఎపిథీలియం యొక్క క్యాన్సర్ రూపాంతరం సమయంలో ప్రదర్శించబడతాయి, ఇది సాధారణంగా HMGCS2 ను వ్యక్తీకరించే సెల్ రకం, మరియు ఇటీవలి నివేదిక HMGCS2 కొలొరెక్టల్ మరియు పొలుసుల కణ క్యాన్సర్లలో పేలవమైన రోగనిర్ధారణకు రోగనిర్ధారణ మార్కర్ అని సూచించింది (కామరెరో మరియు ఇతరులు. 2006; చెన్ మరియు ఇతరులు., 2016). ఈ అనుబంధానికి కీటోజెనిసిస్ అవసరమా లేదా ప్రమేయం ఉందా లేదా HMGCS2 యొక్క మూన్లైటింగ్ ఫంక్షన్ అనేది నిర్ణయించాల్సి ఉంది. దీనికి విరుద్ధంగా, మెలనోమా మరియు గ్లియోబ్లాస్టోమా కణాల ద్వారా OHB ఉత్పత్తి PPARచే ప్రేరేపించబడిందా? అగోనిస్ట్ ఫెనోఫైబ్రేట్, గ్రోత్ అరెస్ట్తో సంబంధం కలిగి ఉంది (గ్రాబాకా మరియు ఇతరులు., 2016). క్యాన్సర్ కణాలలో HMGCS2/SCOT వ్యక్తీకరణ, కీటోజెనిసిస్ మరియు కీటోన్ ఆక్సీకరణ పాత్రలను వర్గీకరించడానికి మరిన్ని అధ్యయనాలు అవసరం.
ఇంధన జీవక్రియ యొక్క పరిధికి మించి, కీటోన్లు ఇటీవల సిగ్నలింగ్ మెకానిజం ద్వారా క్యాన్సర్ కణ జీవశాస్త్రంలో చిక్కుకున్నాయి. BRAF-V600E+ మెలనోమా యొక్క విశ్లేషణ ఆంకోజెనిక్ BRAF-ఆధారిత పద్ధతిలో HMGCL యొక్క OCT1-ఆధారిత ప్రేరణను సూచించింది (కాంగ్ మరియు ఇతరులు., 2015). HMGCL ఆగ్మెంటేషన్ అధిక సెల్యులార్ AcAc ఏకాగ్రతతో పరస్పర సంబంధం కలిగి ఉంది, ఇది BRAFV600E-MEK1 పరస్పర చర్యను మెరుగుపరిచింది, కణితి కణాల విస్తరణ మరియు పెరుగుదలను నడిపించే ఫీడ్-ఫార్వర్డ్ లూప్లో MEK-ERK సిగ్నలింగ్ను విస్తరించింది. ఈ పరిశీలనలు భావి ఎక్స్ట్రాహెపాటిక్ కీటోజెనిసిస్ యొక్క చమత్కారమైన ప్రశ్నను లేవనెత్తుతాయి, అది సిగ్నలింగ్ మెకానిజంకు మద్దతు ఇస్తుంది (అలాగే ?OHBని సిగ్నలింగ్ మధ్యవర్తిగా మరియు ఎక్స్ట్రాహెపాటిక్ కీటోజెనిసిస్లో వివాదాలు కూడా చూడండి). క్యాన్సర్ జీవక్రియపై AcAc, d-?OHB మరియు l-?OHB యొక్క స్వతంత్ర ప్రభావాలను పరిగణనలోకి తీసుకోవడం కూడా చాలా ముఖ్యం మరియు HMGCLని పరిగణనలోకి తీసుకున్నప్పుడు, లూసిన్ క్యాటాబోలిజం కూడా చెదిరిపోవచ్చు.
క్యాన్సర్ జంతు నమూనాలలో కీటోజెనిక్ డైట్ల ప్రభావాలు (కీటోజెనిక్ డైట్ మరియు ఎక్సోజనస్ కీటోన్ బాడీల చికిత్సా ఉపయోగం కూడా చూడండి) వైవిధ్యంగా ఉంటాయి (డి ఫెయిటర్ మరియు ఇతరులు, 2016; క్లెమెంట్ మరియు ఇతరులు., 2016; మీడెన్బౌర్ మరియు ఇతరులు., 2015; పోఫ్ etal. ., 2014; సెయ్ఫ్రైడ్ మరియు ఇతరులు., 2011; శుక్లా మరియు ఇతరులు., 2014). ఊబకాయం, క్యాన్సర్ మరియు కీటోజెనిక్ డైట్ల మధ్య ఎపిడెమియోలాజికల్ అసోసియేషన్లు చర్చనీయాంశమయ్యాయి (లిస్కీవిచ్ మరియు ఇతరులు, 2016; రైట్ మరియు సిమోన్, 2016), జంతు నమూనాలు మరియు మానవ అధ్యయనాలలో కీటోజెనిక్ ఆహారాలను ఉపయోగించి ఒక మెటా-విశ్లేషణ మనుగడపై ప్రయోజనకరమైన ప్రభావాన్ని సూచించింది. కీటోసిస్ యొక్క పరిమాణం, ఆహారం ప్రారంభించే సమయం మరియు కణితి స్థానం (క్లెమెంట్ మరియు ఇతరులు, 2016; వూల్ఫ్ మరియు ఇతరులు., 2016)తో సంభావ్యంగా ప్రయోజనాలు అనుసంధానించబడి ఉంటాయి. కీటోన్ బాడీలతో ప్యాంక్రియాటిక్ క్యాన్సర్ కణాల చికిత్స (d-?OHB లేదా AcAc) పెరుగుదల, విస్తరణ మరియు గ్లైకోలిసిస్ను నిరోధిస్తుంది మరియు కీటోజెనిక్ ఆహారం (81% కిలో కేలరీలు, 18% ప్రోటీన్, 1% కార్బోహైడ్రేట్) వివో ట్యూమర్ బరువు, గ్లైసెమియా మరియు అమర్చిన క్యాన్సర్ ఉన్న జంతువులలో పెరిగిన కండరాలు మరియు శరీర బరువు (శుక్లా మరియు ఇతరులు, 2014). ఆహారంలో కీటోన్ సప్లిమెంటేషన్ పొందిన ఎలుకలలో మెటాస్టాటిక్ గ్లియోబ్లాస్టోమా సెల్ మోడల్ను ఉపయోగించి ఇలాంటి ఫలితాలు గమనించబడ్డాయి (పాఫ్ మరియు ఇతరులు., 2014). దీనికి విరుద్ధంగా, కీటోజెనిక్ ఆహారం (91% కిలో కేలరీలు కొవ్వు, 9% ప్రోటీన్) ప్రసరణను పెంచింది ?OHB ఏకాగ్రత మరియు క్షీణించిన గ్లైసెమియా, కానీ గ్లియోమా-బేరింగ్ ఎలుకలలో కణితి పరిమాణం లేదా మనుగడ వ్యవధిపై ప్రభావం చూపలేదు (డి ఫెయిటర్ మరియు ఇతరులు., 2016). మానవులు మరియు ఎలుకలలో కీటోజెనిక్ డైట్-ప్రేరిత మెదడు క్యాన్సర్ చికిత్స యొక్క జీవక్రియ నిర్వహణను మెరుగుపరిచే క్లినికల్ సూచికగా గ్లూకోజ్ కీటోన్ ఇండెక్స్ ప్రతిపాదించబడింది (మీడెన్బౌర్ మరియు ఇతరులు., 2015). కలిసి తీసుకుంటే, క్యాన్సర్ జీవశాస్త్రంలో కీటోన్ బాడీ మెటబాలిజం మరియు కీటోన్ బాడీల పాత్రలు ప్రేరేపిస్తాయి ఎందుకంటే అవి ప్రతి ఒక్కటి ట్రాక్టబుల్ చికిత్సా ఎంపికలను కలిగి ఉంటాయి, అయితే ప్రాథమిక అంశాలు విశదీకరించబడాలి, వేరియబుల్స్ యొక్క మాతృక నుండి స్పష్టమైన ప్రభావాలు వెలువడుతున్నాయి, వీటిలో (i) ఎక్సోజనస్ కీటోన్ మధ్య తేడాలు ఉన్నాయి. శరీరాలు వర్సెస్ కీటోజెనిక్ డైట్, (ii) క్యాన్సర్ కణ రకం, జెనోమిక్ పాలిమార్ఫిజమ్స్, గ్రేడ్ మరియు స్టేజ్; మరియు (iii) కీటోటిక్ స్థితికి బహిర్గతమయ్యే సమయం మరియు వ్యవధి.

కీటోజెనిసిస్ అనేది కొవ్వు ఆమ్లాలు మరియు కీటోజెనిక్ అమైనో ఆమ్లాల విచ్ఛిన్నం ద్వారా కీటోన్ శరీరాలచే సృష్టించబడుతుంది. ఈ జీవరసాయన ప్రక్రియ వివిధ అవయవాలకు, ప్రత్యేకంగా మెదడుకు, రక్తంలో గ్లూకోజ్ లభ్యతకు ప్రతిస్పందనగా ఉపవాస పరిస్థితులలో శక్తిని అందిస్తుంది. కీటోన్ శరీరాలు ప్రధానంగా కాలేయ కణాల మైటోకాండ్రియాలో ఉత్పత్తి అవుతాయి. ఇతర కణాలు కీటోజెనిసిస్ను నిర్వహించగల సామర్థ్యాన్ని కలిగి ఉన్నప్పటికీ, అవి కాలేయ కణాల వలె ప్రభావవంతంగా ఉండవు. మైటోకాండ్రియాలో కీటోజెనిసిస్ సంభవిస్తుంది కాబట్టి, దాని ప్రక్రియలు స్వతంత్రంగా నియంత్రించబడతాయి. డాక్టర్ అలెక్స్ జిమెనెజ్ DC, CCST ఇన్సైట్
కీటోజెనిక్ డైట్ మరియు ఎక్సోజనస్ కీటోన్ బాడీస్ యొక్క చికిత్సా అప్లికేషన్
స్థూలకాయం మరియు NAFLD/NASH (బ్రౌనింగ్ et al., 2011; Foster et al., 2010; Schugar and Crawford, 2012)తో సహా క్యాన్సర్ లేని సందర్భాలలో కూడా కీటోజెనిక్ డైట్లు మరియు కీటోన్ బాడీలను చికిత్సా సాధనాలుగా ఉపయోగించడం ప్రారంభించింది; గుండె వైఫల్యం (హుయిన్, 2016; కోల్విజ్ మరియు ఇతరులు, 2016; తాగ్ట్మేయర్, 2016); న్యూరోలాజికల్ మరియు న్యూరోడెజెనరేటివ్ డిసీజ్ (మార్టిన్ మరియు ఇతరులు, 2016; మెక్నల్లీ మరియు హార్ట్మన్, 2012; రో, 2015; రోగావ్స్కీ మరియు ఇతరులు., 2016; యాంగ్ మరియు చెంగ్, 2010; యావో మరియు ఇతరులు., 2011); జీవక్రియ యొక్క పుట్టుకతో వచ్చే లోపాలు (స్కోల్-బర్గి మరియు ఇతరులు, 2015); మరియు వ్యాయామ పనితీరు (కాక్స్ మరియు ఇతరులు, 2016). ఎపిలెప్టిక్ మూర్ఛ యొక్క చికిత్సలో, ముఖ్యంగా ఔషధ-నిరోధక రోగులలో కీటోజెనిక్ ఆహారాల యొక్క సమర్థత ప్రత్యేకంగా ప్రశంసించబడింది. చాలా అధ్యయనాలు పీడియాట్రిక్ రోగులలో కీటోజెనిక్ డైట్లను మూల్యాంకనం చేశాయి మరియు 50 నెలల తర్వాత మూర్ఛ ఫ్రీక్వెన్సీలో ~3% తగ్గింపును వెల్లడిస్తున్నాయి, ఎంపిక చేసిన సిండ్రోమ్లలో మెరుగైన ప్రభావంతో (Wu et al., 2016b). వయోజన మూర్ఛలో అనుభవం చాలా పరిమితంగా ఉంటుంది, అయితే ఇదే విధమైన తగ్గింపు స్పష్టంగా కనిపిస్తుంది, రోగలక్షణ సాధారణీకరించిన మూర్ఛ రోగులలో మెరుగైన ప్రతిస్పందన (Nei et al., 2014). తగ్గిన గ్లూకోజ్ వినియోగం/గ్లైకోలిసిస్, రీప్రోగ్రామ్ చేయబడిన గ్లూటామేట్ రవాణా, ATP-సెన్సిటివ్ పొటాషియం ఛానల్ లేదా అడెనోసిన్ A1 రిసెప్టర్పై పరోక్ష ప్రభావం, సోడియం ఛానల్ ఐసోఫార్మ్ ఎక్స్ప్రెషన్లో మార్పు (లేదా సర్క్యులేటింగ్ హార్మోన్తో సహా హార్మోన్ల ప్రభావాలు) వంటి అంశాలు సూచించబడినప్పటికీ, అంతర్లీన యాంటీ కన్వల్సెంట్ మెకానిజమ్స్ అస్పష్టంగానే ఉన్నాయి. Lambrechts et al., 2016; Lin et al., 2017; Lutas and Yellen, 2013). యాంటీ కన్వల్సెంట్ ఎఫెక్ట్ ప్రధానంగా కీటోన్ బాడీలకు ఆపాదించబడుతుందా లేదా తక్కువ కార్బోహైడ్రేట్ డైట్ల క్యాస్కేడ్ మెటబాలిక్ పర్యవసానాల వల్లా అనేది అస్పష్టంగానే ఉంది. ఏది ఏమైనప్పటికీ, కీటోన్ ఈస్టర్లు (క్రింద చూడండి) రెచ్చగొట్టబడిన మూర్ఛల యొక్క జంతు నమూనాలలో నిర్భందించటం థ్రెషోల్డ్ను పెంచడం కనిపిస్తుంది (Ciarlone et al., 2016; D'Agostino et al., 2013; Viggiano et al., 2015).
అట్కిన్స్-శైలి మరియు కీటోజెనిక్, తక్కువ కార్బోహైడ్రేట్ ఆహారాలు తరచుగా అసహ్యకరమైనవిగా పరిగణించబడతాయి మరియు మలబద్ధకం, హైపర్యూరిసెమియా, హైపోకాల్సెమియా, హైపోమాగ్నేసిమియా, నెఫ్రోలిథియాసిస్, కీటోయాసిడోసిస్, హైపర్గ్లైసీమియాకు కారణమవుతాయి మరియు ప్రసరించే కొలెస్ట్రాల్ మరియు ఉచిత కొవ్వు ఆమ్ల సాంద్రత, 2001 బి. ; కోసోఫ్ మరియు హార్ట్మన్, 2012; క్విటెరోవిచ్ మరియు ఇతరులు., 2003; సుజుకి మరియు ఇతరులు., 2002). ఈ కారణాల వల్ల, దీర్ఘకాలిక కట్టుబడి ఉండటం సవాళ్లను కలిగిస్తుంది. ఎలుకల అధ్యయనాలు సాధారణంగా విలక్షణమైన మాక్రోన్యూట్రియెంట్ పంపిణీని ఉపయోగిస్తాయి (94% కిలో కేలరీలు, 1% కిలో కేలరీలు కార్బోహైడ్రేట్, 5% కిలో కేలరీలు ప్రోటీన్, బయో-సర్వ్ F3666), ఇది బలమైన కీటోసిస్ను రేకెత్తిస్తుంది. అయినప్పటికీ, ప్రోటీన్ కంటెంట్ను 10% కిలో కేలరీలు పెంచడం వల్ల కీటోసిస్ను గణనీయంగా తగ్గిస్తుంది మరియు 5% కిలో కేలరీల ప్రోటీన్ పరిమితి గందరగోళంగా జీవక్రియ మరియు శారీరక ప్రభావాలను అందిస్తుంది. ఈ డైట్ ఫార్ములేషన్ కూడా కోలిన్ క్షీణించింది, కాలేయ గాయానికి గురికావడాన్ని ప్రభావితం చేసే మరొక వేరియబుల్ మరియు కీటోజెనిసిస్ కూడా (గార్బో మరియు ఇతరులు, 2011; జోర్నైవాజ్ మరియు ఇతరులు., 2010; కెన్నెడీ మరియు ఇతరులు., 2007; పిస్సియోస్ మరియు ఇతరులు 2013;, ఇతరులు. మరియు ఇతరులు, 2013). ఎలుకలలో కీటోజెనిక్ ఆహారం యొక్క దీర్ఘకాలిక వినియోగం యొక్క ప్రభావాలు అసంపూర్ణంగా నిర్వచించబడ్డాయి, అయితే ఎలుకలలో ఇటీవలి అధ్యయనాలు సాధారణ మనుగడను మరియు ఎలుకలలో కాలేయ గాయం గుర్తులు లేకపోవడాన్ని వారి జీవితకాలంలో కెటోజెనిక్ ఆహారంలో వెల్లడించాయి, అయినప్పటికీ అమైనో ఆమ్లం జీవక్రియ, శక్తి వ్యయం మరియు ఇన్సులిన్ సిగ్నలింగ్ గుర్తించదగిన రీప్రోగ్రామ్ చేయబడ్డాయి (డౌరిస్ మరియు ఇతరులు, 2015).
కీటోజెనిక్ డైట్లకు ప్రత్యామ్నాయంగా మెకానిజమ్స్ ద్వారా కీటోసిస్ను పెంచే మెకానిజమ్స్లో ఇన్జెస్టబుల్ కీటోన్ బాడీ పూర్వగాములు ఉపయోగించబడతాయి. ఎక్సోజనస్ కీటోన్ బాడీల నిర్వహణ సాధారణ శరీరధర్మ శాస్త్రంలో లేని ప్రత్యేకమైన శారీరక స్థితిని సృష్టించగలదు, ఎందుకంటే గ్లూకోజ్ మరియు ఇన్సులిన్ సాంద్రతలు ప్రసరణ సాపేక్షంగా సాధారణం, అయితే కణాలు గ్లూకోజ్ తీసుకోవడం మరియు వినియోగాన్ని విడిచిపెట్టవచ్చు. కీటోన్ శరీరాలు తక్కువ అర్ధ-జీవితాన్ని కలిగి ఉంటాయి మరియు చికిత్సా కీటోసిస్ను సాధించడానికి సోడియం ?OHB ఉప్పును తీసుకోవడం లేదా కషాయం చేయడం వలన అవాంఛనీయమైన సోడియం లోడ్ను రేకెత్తిస్తుంది. R/S-1,3-butanediol అనేది నాన్-టాక్సిక్ డయల్ ఆల్కహాల్, ఇది d/l-?OHB (Desrochers et al., 1992) ఇవ్వడానికి కాలేయంలో తక్షణమే ఆక్సీకరణం చెందుతుంది. విభిన్న ప్రయోగాత్మక సందర్భాలలో, ఈ మోతాదు ప్రతిరోజూ ఎలుకలు లేదా ఎలుకలకు ఏడు వారాలపాటు అందించబడుతుంది, ఇది పరిపాలన యొక్క 5 గంటలలోపు 2 mM వరకు ?OHB సాంద్రతలను అందిస్తుంది, ఇది కనీసం అదనపు 3h (D') వరకు స్థిరంగా ఉంటుంది. అగోస్టినో మరియు ఇతరులు., 2013). R/S-1,3-butanediol (కార్పెంటర్ మరియు గ్రాస్మాన్, 1983) ఇచ్చిన ఎలుకలలో ఆహారం తీసుకోవడం పాక్షికంగా అణచివేయడం గమనించబడింది. అదనంగా, మూడు రసాయనికంగా విభిన్నమైన కీటోన్ ఈస్టర్లు (KEs), (i) R-1,3-బ్యూటానెడియోల్ మరియు d-?OHB (R-3-హైడ్రాక్సీబ్యూటిల్ R-?OHB) యొక్క మోనోస్టర్; (ii) గ్లిసరిల్-ట్రిస్-?OHB; మరియు (iii) R,S-1,3-butanediol అసిటోఅసిటేట్ డైస్టర్, కూడా విస్తృతంగా అధ్యయనం చేయబడింది (బ్రూనెన్గ్రాబర్, 1997; క్లార్క్ మరియు ఇతరులు, 2012a; క్లార్క్ మరియు ఇతరులు., 2012b; డెస్రోచెర్స్ మరియు ఇతరులు., 1995a; ., 1995b; కాశివాయ మరియు ఇతరులు., 2010). పూర్వం యొక్క స్వాభావిక ప్రయోజనం ఏమిటంటే, పేగు లేదా కాలేయంలో ఎస్టేరేస్ జలవిశ్లేషణను అనుసరించి, KE యొక్క మోల్కు 2 మోల్స్ ఫిజియోలాజికల్ d-?OHB ఉత్పత్తి అవుతాయి. R-3-హైడ్రాక్సీబ్యూటిల్ R-?OHB, 714 mg/kg వరకు మోతాదులో, 6 mM వరకు ప్రసరణ d-?OHB సాంద్రతలను అందజేసే మానవులలో భద్రత, ఫార్మకోకైనటిక్స్ మరియు సహనం చాలా విస్తృతంగా అధ్యయనం చేయబడ్డాయి (క్లార్క్ మరియు ఇతరులు., 2012a; కాక్స్ మరియు ఇతరులు., 2016; కెంపర్ మరియు ఇతరులు., 2015; శివ్వా మరియు ఇతరులు., 2016). ఎలుకలలో, ఈ KE కేలరీల తీసుకోవడం మరియు ప్లాస్మా మొత్తం కొలెస్ట్రాల్ను తగ్గిస్తుంది, బ్రౌన్ కొవ్వు కణజాలాన్ని ప్రేరేపిస్తుంది మరియు ఇన్సులిన్ నిరోధకతను మెరుగుపరుస్తుంది (కాశీవాయ మరియు ఇతరులు, 2010; కెంపర్ మరియు ఇతరులు., 2015; వీచ్, 2013). శిక్షణ పొందిన అథ్లెట్లలో వ్యాయామం చేస్తున్నప్పుడు, R-3-హైడ్రాక్సీబ్యూటిల్ R-?OHB తీసుకోవడం వల్ల అస్థిపంజర కండరాల గ్లైకోలిసిస్ మరియు ప్లాస్మా లాక్టేట్ సాంద్రతలు తగ్గాయి, ఇంట్రామస్కులర్ ట్రైయాసిల్గ్లిసరాల్ ఆక్సీకరణం మరియు సంరక్షించబడిన కండరాల గ్లైకోజెన్ కంటెంట్, సహ-ప్రేరేపిత కార్బోహైడ్రేట్ స్రవించినప్పటికీ, శిక్షణ పొందిన అథ్లెట్లలో వ్యాయామం చేయడాన్ని ఇటీవలి పరిశోధనలు సూచిస్తున్నాయి. కాక్స్ మరియు ఇతరులు., 2016). ఈ చమత్కార ఫలితాల యొక్క మరింత అభివృద్ధి అవసరం, ఎందుకంటే ఓర్పు వ్యాయామ పనితీరులో మెరుగుదల ప్రధానంగా 2/8 విషయాలలో KEకి బలమైన ప్రతిస్పందన ద్వారా నడపబడుతుంది. అయినప్పటికీ, ఈ ఫలితాలు ఇతర సబ్స్ట్రేట్ల కంటే కీటోన్ ఆక్సీకరణకు ప్రాధాన్యతనిచ్చే శాస్త్రీయ అధ్యయనాలకు మద్దతు ఇస్తాయి (గార్లాండ్ మరియు ఇతరులు, 1962; హాసెల్బైంక్ మరియు ఇతరులు., 2003; స్టాన్లీ మరియు ఇతరులు., 2003; వాలెంటె-సిల్వా మరియు ఇతరులు., 2015), వ్యాయామ సమయంలో సహా, మరియు శిక్షణ పొందిన అథ్లెట్లు కీటోన్లను ఉపయోగించుకోవడానికి మరింత ప్రాధాన్యతనిస్తారు (జాన్సన్ మరియు ఇతరులు, 1969a; జాన్సన్ మరియు వాల్టన్, 1972; విండర్ మరియు ఇతరులు., 1974; విండర్ మరియు ఇతరులు., 1975). చివరగా, సమాన కేలరీల తీసుకోవడం (స్థూల పోషకాల మధ్య విభిన్నంగా పంపిణీ) మరియు సమాన ఆక్సిజన్ వినియోగ రేట్లు తర్వాత మెరుగైన వ్యాయామ పనితీరుకు మద్దతు ఇచ్చే యంత్రాంగాలు నిర్ణయించబడతాయి.
భవిష్యత్తు దృక్పథం
కార్బోహైడ్రేట్ నిరోధిత స్థితులలో ('కీటోటాక్సిక్' నమూనా) కొవ్వు దహనం నుండి విషపూరిత ఉద్గారాలను పేరుకుపోయే సామర్థ్యం కలిగిన ఓవర్ఫ్లో మార్గంగా ఒకసారి ఎక్కువగా కళంకం కలిగింది, ఇటీవలి పరిశీలనలు కార్బోహైడ్రేట్-లాడెన్ స్టేట్స్లో కూడా కీటోన్ బాడీ మెటబాలిజం ప్రయోజనకరమైన పాత్రలను పోషిస్తుందనే భావనకు మద్దతు ఇస్తుంది. --- పరికల్పన. కీటోన్ జీవక్రియను మార్చటానికి సులభమైన పోషకాహార మరియు ఔషధ విధానాలు దానిని ఆకర్షణీయమైన చికిత్సా లక్ష్యంగా మార్చినప్పటికీ, దూకుడుగా చూపబడినప్పటికీ వివేకవంతమైన ప్రయోగాలు ప్రాథమిక మరియు అనువాద పరిశోధనా ప్రయోగశాలలు రెండింటిలోనూ ఉన్నాయి. గుండె వైఫల్యం, ఊబకాయం, NAFLD/NASH, టైప్ 2 మధుమేహం మరియు క్యాన్సర్లో కీటోన్ జీవక్రియను ప్రభావితం చేసే పాత్రను నిర్వచించే డొమైన్లలో అన్మెట్ అవసరాలు ఉద్భవించాయి. కీటోన్ బాడీల యొక్క 'కానానికల్-కాని' సిగ్నలింగ్ పాత్రల యొక్క పరిధి మరియు ప్రభావం, PTMల నియంత్రణతో సహా, జీవక్రియ మరియు సిగ్నలింగ్ మార్గాల్లోకి తిరిగి మరియు ముందుకు వెళ్లే అవకాశం ఉంది, లోతైన అన్వేషణ అవసరం. చివరగా, ఎక్స్ట్రాహెపాటిక్ కీటోజెనిసిస్ చమత్కారమైన పారాక్రిన్ మరియు ఆటోక్రిన్ సిగ్నలింగ్ మెకానిజమ్స్ మరియు నాడీ వ్యవస్థలో సహ-జీవక్రియను ప్రభావితం చేసే అవకాశాలను మరియు చికిత్సా చివరలను సాధించడానికి కణితులను తెరవగలదు.
అందినట్లు
Ncbi.nlm.nih.gov/pmc/articles/PMC5313038/
ఫుట్నోట్స్
ముగింపులో, మానవ శరీరంలో తగినంత గ్లూకోజ్ తక్షణమే అందుబాటులో లేనప్పుడు శక్తి వనరుగా ఉపయోగించేందుకు కీటోన్ శరీరాలు కాలేయం ద్వారా సృష్టించబడతాయి. రక్తంలో తక్కువ గ్లూకోజ్ స్థాయిలు ఉన్నప్పుడు, ముఖ్యంగా ఇతర సెల్యులార్ కార్బోహైడ్రేట్ దుకాణాలు అయిపోయిన తర్వాత కీటోజెనిసిస్ సంభవిస్తుంది. ఇంధన జీవక్రియ, సిగ్నలింగ్ మరియు థెరప్యూటిక్స్లో కీటోన్ బాడీల యొక్క బహుళ-డైమెన్షనల్ పాత్రలను చర్చించడం పై కథనం యొక్క ఉద్దేశ్యం. మా సమాచారం యొక్క పరిధి చిరోప్రాక్టిక్ మరియు వెన్నెముక ఆరోగ్య సమస్యలకు పరిమితం చేయబడింది. విషయం గురించి చర్చించడానికి, దయచేసి డాక్టర్ జిమెనెజ్ని అడగడానికి సంకోచించకండి లేదా మమ్మల్ని సంప్రదించండి915-850-0900 .
డా. అలెక్స్ జిమెనెజ్చే నిర్వహించబడింది
దీని నుండి సూచించబడింది:Ncbi.nlm.nih.gov/pmc/articles/PMC5313038/

అదనపు టాపిక్ చర్చ: తీవ్రమైన వెన్నునొప్పి
వెన్నునొప్పిప్రపంచవ్యాప్తంగా వైకల్యం మరియు పనిలో రోజులు తప్పిపోవడానికి అత్యంత ప్రబలమైన కారణాలలో ఒకటి. వెన్నునొప్పి వైద్యుని కార్యాలయ సందర్శనలకు రెండవ అత్యంత సాధారణ కారణం, ఎగువ శ్వాసకోశ ఇన్ఫెక్షన్ల సంఖ్య కంటే ఎక్కువగా ఉంటుంది. జనాభాలో సుమారు 80 శాతం మంది తమ జీవితాంతం ఒక్కసారైనా వెన్నునొప్పిని అనుభవిస్తారు. వెన్నెముక అనేది ఇతర మృదు కణజాలాలలో ఎముకలు, కీళ్ళు, స్నాయువులు మరియు కండరాలతో కూడిన సంక్లిష్టమైన నిర్మాణం. గాయాలు మరియు/లేదా తీవ్రమైన పరిస్థితులు, వంటివిహెర్నియేటెడ్ డిస్క్లు, చివరికి వెన్నునొప్పి యొక్క లక్షణాలకు దారితీయవచ్చు. స్పోర్ట్స్ గాయాలు లేదా ఆటోమొబైల్ ప్రమాద గాయాలు తరచుగా వెన్నునొప్పికి చాలా తరచుగా కారణం, అయినప్పటికీ, కొన్నిసార్లు సరళమైన కదలికలు బాధాకరమైన ఫలితాలను కలిగి ఉంటాయి. అదృష్టవశాత్తూ, చిరోప్రాక్టిక్ కేర్ వంటి ప్రత్యామ్నాయ చికిత్సా ఎంపికలు, వెన్నెముక సర్దుబాట్లు మరియు మాన్యువల్ మానిప్యులేషన్స్ ఉపయోగించడం ద్వారా వెన్నునొప్పిని తగ్గించడంలో సహాయపడతాయి, చివరికి నొప్పి నివారణను మెరుగుపరుస్తాయి. �

అదనపు అదనపు | ముఖ్యమైన అంశం: సిఫార్సు చేయబడిన ఎల్ పాసో, TX చిరోప్రాక్టర్
***